Ⅰ.工业上常用电解饱和食盐水的方法制备氯气 其装置如图1所示 如果在饱和食盐水中滴加酚酞 通电后__
| Ⅰ.工业上常用电解饱和食盐水的方法制备氯气,其装置如图1所示,如果在饱和食盐水中滴加酚酞,通电后______ (填X或Y)极附近溶液变红,写出电解饱和食盐水的化学方程式______.再用氯气制备漂白粉,请写出漂白粉长期露置在空气中失效的反应的化学方程式______. Ⅱ.请利用图2装置及试剂组装一套装置,其流程是先制取纯净干燥的Cl2(不收集),后试验干燥的Cl2和潮湿的Cl2有无漂白性. 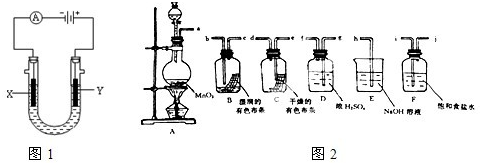 (1)按气体从左向右流向将各装置依次连接起来(填接口标号):a 接______,______接______,______接______,______接______,______接______. (2)圆底烧瓶中发生反应的化学方程式是______.如果将过量二氧化锰与20mL 12mol?L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol.其主要原因为______. (3)E装置的作用是______,F装置的作用是______. (4)装置______(填“B”或“C”)中的有色布条褪色,以上事实说明起漂白作用的物质是______. |
参考解答
Ⅰ.电解饱和食盐水的方法制备氯气,装置图中与电源正极连接的Y电极为阳极,溶液中氯离子失电子发生氧化反应生成氯气,与电源负极连接的X电极为电解池的阴极,溶液中氢离子得到电子发生还原反应,生成氢气,反应的化学方程式为2NaCl+2H2O
Ⅱ.(1)验装置的连接顺序为:发生装置→除杂装置→性质检验装置→尾气处理装置;因为收集的是气体,所以除杂装置中长导管进气,段导管出气;因为饱和食盐水中有水,浓硫酸有吸水性,所以先连接饱和食盐水装置后连接浓硫酸装置;试验干燥的Cl2和潮湿的Cl2有无漂白性,因为湿润的有色布条有水分,所以D装置先连接C后连接B, 故答案为:a→i→j→g→f→e→d→b→c→h; (2)浓盐酸有还原性,二氧化锰有氧化性,浓盐酸和二氧化锰能发生氧化还原反应生成氯化锰、氯气和水.随反应进行,浓盐酸浓度减小变稀后不能和二氧化锰反应生成氯气, 故答案为:MnO2+4HCl(浓)
(3)浓盐酸有挥发性,浓盐酸中的水在加热的条件下变成水蒸气,所以氯气中混有氯化氢和水蒸气;氯气有毒,污染环境,所以不能直接排空;氯气能和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以可用氢氧化钠溶液吸收多余的氯气.氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl2+H2O=H++Cl-+HClO,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和的食盐水除去HCl气体, 故答案为:吸收多余的氯气防止污染空气;除去氯气中的HCl气体; (4)氯气能水反应,反应方程式为:Cl2+H2O=H++Cl-+HClO,C瓶中的成分是氯气,不能使有色布条褪色,BB瓶中有次氯酸生成,使有色布条褪色,以上事实说明起漂白作用的物质是次氯酸,故答案为:B,次氯酸(HClO). |
相似问题
如图X Y分别是直流电源的两极 通电后发现a极板质量增加 d极板有无色无臭的气体放出 符合这一情况的
如图X、Y分别是直流电源的两极,通电后发现a极板质量增加,d极板有无色无臭的气体放出,符合这一情况的是( )选项a极板d极板X极板乙中溶液A锌铜负极C
高功率Ni/MH(M表示储氢合金 MH中的H可看作0价)电池已经用于混合动力汽车。总反应方程式如下:
高功率Ni MH(M表示储氢合金,MH中的H可看作0价)电池已经用于混合动力汽车。总反应方程式如下:Ni(OH)2+MNiOOH+MH 下列叙述正确的是 [ ]A 放电时正
近年来 加“碘”食盐较多使用了碘酸钾 KIO3在工业上可用电解法制取 以石墨和铁为电极 以KI溶液为
近年来,加“碘”食盐较多使用了碘酸钾,KIO3在工业上可用电解法制取,以石墨和铁为电极,以KI溶液为电解液在一定条件下电解,反应式为:KI+H2O→KIO3+H2
以惰性电极电解CuSO4溶液.若阳极上产生气体的物质的量为0.01mol 则阴极上析出Cu的质量为(
以惰性电极电解CuSO4溶液.若阳极上产生气体的物质的量为0 01mol,则阴极上析出Cu的质量为( )A.0 64gB.1 28gC.2 56gD.5 12g
右图表示一个电解池 电解液ɑ是足量的饱和NaCl溶液 X Y都是石墨电极 实验开始前 在两边各滴入几
右图表示一个电解池,电解液ɑ是足量的饱和NaCl溶液,X、Y都是石墨电极,实验开始前,在两边各滴入几滴酚酞试液,则:(1)X电极上的电极反应式为______












