(14分)按要求回答下列问题:(1)石墨晶体中C-C键的键角为 _____。其中平均每个六边形所
| (14分)按要求回答下列问题: (1)石墨晶体中C-C键的键角为 _____。其中平均每个六边形所含的C原子数为 个。 (2)金刚石晶体中含有共价键形成的C原子环,其中最小的C环上有 个C原子。 (3)CsCl晶体中每个Cs+周围有 个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有 个。 (4)白磷分子中的键角为 ,分子的空间结构为 ,每个P原子与 个P原子结合成共价键。若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合 个氧原子, 若每个P原子上的孤对电子再与氧原子配位,就可以得到磷的另一种氧化物 (填分子式)。 (5)二氧化硅是一种 晶体,每个硅原子周围有 个氧原子。 (6)晶体硼的基本结构单元是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答:这个基本结构单元由_____个硼原子组成,共含有________个B-B键。 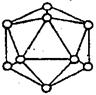 |
参考解答
| (1)120°; 2。 (2)6 (3)8; 6 (每空1分) (4)60°;正四面体; 3; 6; P4O10。 (5)原子; 4。 (6)12; 30。 |
| 考查常见的晶体结构类型。 (1)石墨是层状结构,石墨晶体中C-C键的键角为120°。由于每个碳原子被3个正六边形共用,所以平均每个六边形所含的C原子数为6×1/3=2个。 (2)金刚石晶体中最小的C环上有6个碳原子。 (3)氯化铯晶体的配位数是8,所以CsCl晶体中每个Cs+周围有8个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有6个,即上下、前后、左右个一个。 (4)白磷是正四面体型结构,键角是60°。每个P原子与3个P原子结合成共价键。由于分子中共有6个P-P键,所以需要插入6个氧原子。若每个P原子上的孤对电子再与氧原子配位,则又可以结合4个氧原子,所以化学式为P4O10。 (5)二氧化硅是一种原子晶体,由于每个硅原子钠形成4和Si-O键,所以每个硅原子周围有4个氧原子。 (6)根据结构可知,每个B原子被5个相邻的三角形共用,所以含有的B原子是3×1/5×20=12。每个B-B键被2个相邻的三角形共用,所以含有的B-B键是3×1/2×20=30。 |
相似问题
下列分子或离子中都存在着配位键的是( )A.NH3 H2OB.NH4+ H3O+C.N2 HClO
下列分子或离子中都存在着配位键的是( )A.NH3、H2OB.NH4+、H3O+C.N2、HClOD.[Cu(NH3)4]2+、PCl3
与氖(Ne)原子电子排布相同的两种离子组成的化合物是( )A.Na2SB.KClC.MgCl2D.N
与氖(Ne)原子电子排布相同的两种离子组成的化合物是()A.Na2SB.KClC.MgCl2D.NaF
下列物质中 既有离子键又有共价键的是A.Ca(NO3)2 B.KOHC.H2OD.NH4F
下列物质中,既有离子键又有共价键的是A.Ca(NO3)2 B.KOHC.H2OD.NH4F
(10分)在NaCl NaOH N2 H2S Na2O2中 只含有离子键的是 只含有极性
(10分)在NaCl、NaOH、N2、H2S、Na2O2中,只含有离子键的是,只含有极性键的是,只含有非极性键的是,既含有离子键又有极性键的是,既含有离子键又有非
(8分)有以下物质:①HF ②Cl2 ③H2O ④N2 ⑤C2H4 ⑥C2H6 ⑦H2 ⑧H2O2
(8分)有以下物质:①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥C2H6,⑦H2,⑧H2O2,⑨HCN(H—C≡N);(1)只含有极性键的是__________;只含有非极性键的是_












