常见元素A B C D 其原子结构的相关信息如下表:元素相关信息AA原子的核外电子总数等于其基态电子
常见元素A、B、C、D,其原子结构的相关信息如下表:
请回答下列问题: (1)A的原子结构示意图是_______;D元素位于周期表第______周期 ______族。 (2)在由B和A形成的众多分子中,只要B原子的成键轨道满足______(填字母序号),分子中所有的原子就有可能在同一个平面内。 A.sp3或sp2杂化轨道 B.sp3或sp杂化轨道 C.sp或sp2杂化轨道 (3)如图,在B晶体的一个晶胞中含有______个B原子。 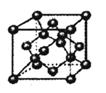 (4)制备C2A4的方法是用次氯酸钠(NaClO)溶液氧化过量的CA3。 ①CA3分子是______(填“极性”或“非极性”)分子。 ②写出制备C2A4的总反应方程式____________ (5)DC13晶体溶于水溶液呈酸性,其原因是(用离子方程式表示):______________________________ |
参考解答
| (16分) (1) 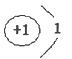 (2分);四 (1分) Ⅷ (1分) (2分);四 (1分) Ⅷ (1分)(2)C (2分) (3)8 (2分) (4)①极性 (2分) ②NaClO+2NH3=N2H4+NaCl+H2O (3分) (5)Fe3++3H2O  Fe(OH)3+3H+ (3分) Fe(OH)3+3H+ (3分) |
试题分析:根据题意可知A、B、C、D分别为H、C、N、Fe。 (2)sp2为平面结构,sp3为直线型结构,故均共面,答案为A (3)从图中可以看出,C的位置有三种,分别为顶点、面心、体心,为8× 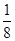 +6× +6×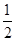 +4×1=8 +4×1=8(4)NH3为三角锥形,故为极性分子;根据反应物和产物结合氧化还原反应配平的方法,可以得到。 (3)FeCl3为强酸弱碱盐,水解呈酸性。 |
相似问题
X Y Z R W均为周期表中前四周期的元素 其原子序数依次增大;x2-和Y+有相同的核外电子排布;
X、Y、Z、R、W均为周期表中前四周期的元素,其原子序数依次增大;x2-和Y+有相同的核外电子排布;Z的氢化物的沸点比其上一周期同族元素氢化物的沸点低;R
铬 铁 镍 铜等金属及其化合物在工业上有重要用途。(1)基态铬原子的价电子排布式为
铬、铁、镍、铜等金属及其化合物在工业上有重要用途。(1)基态铬原子的价电子排布式为。(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2C
(1)Fe3+可以与SCN- CN- F- 有机分子等形成很多的配合物。①写出基态Fe3+的核外电子
(1)Fe3+可以与SCN-、CN-、F-、有机分子等形成很多的配合物。①写出基态Fe3+的核外电子排布式。②已知(CN)2是直线型分子,并有对称性,则(CN)2中π键和
A B C D E F为原子序数依次增大的短周期主族元素。已知:A C F 3种元素原子的最外层共有
A,B,C,D,E,F为原子序数依次增大的短周期主族元素。已知:A,C,F 3种元素原子的最外层共有11个电子,且这3种元素的最高价氧化物对应水化物之间两两
X Y Z W是元素周期表前四周期中的四种常见元素 其相关信息如下表(1)Y位于元素周期表第____
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表(1)Y位于元素周期表第_____周期_____族,Y和Z的最高价氧化物对应的水化物的酸性较












