将煤气化转化成合成气 然后通过一碳化工路线合成各种油品和石化产品是一碳化工的极为重要的领域 具有广阔
| 将煤气化转化成合成气,然后通过一碳化工路线合成各种油品和石化产品是一碳化工的极为重要的领域,具有广阔的前景,在未来相当一段时期将成为一碳化工的主要领域。 除去水蒸气后的水煤气含55~59%的H2,15~18%的CO,11~13%的CO2,少量的H2S、CH4,除去H2S后,可采用催化或非催化转化技术,将CH4转化成CO,得到CO、CO2和H2的混合气体,是理想的合成甲醇原料气,即可进行甲醇合成。 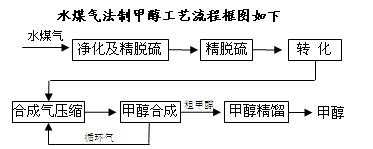 (1)制水煤气的主要化学反应方程式为:C(s)+H2O(g)  CO(g)+H2(g),此反应是 CO(g)+H2(g),此反应是吸热反应。 ① 此反应的化学平衡常数表达式为, ; ②下列能增大碳的转化率的措施是 ;
CH4 (g)+3/2O2 (g)  CO (g)+2H2O (g) △H=-519KJ/mol。工业上要选择合适的催化剂,分别对X、Y、Z三种催化剂进行如下实验(其他条件相同) CO (g)+2H2O (g) △H=-519KJ/mol。工业上要选择合适的催化剂,分别对X、Y、Z三种催化剂进行如下实验(其他条件相同)① X在T1℃时催化效率最高,能使正反应速率加快约3×105倍; ② Y在T2℃时催化效率最高,能使正反应速率加快约3×105倍; ③ Z在T3℃时催化效率最高,能使逆反应速率加快约1×106倍; 已知:T1>T2>T3,根据上述信息,你认为在生产中应该选择的适宜催化剂是 (填“X”或“Y”或“Z”),选择的理由是 ; (3)合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,进行甲醇合成,主要反应如下: 2H2(g) + CO(g)  CH3OH(g);ΔH =-90.8kJ·mol-1,T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下: CH3OH(g);ΔH =-90.8kJ·mol-1,T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
② 若加入CO、H2后,在T5℃反应10min达到平衡,c(H2)=0.4 mol·L-1,则该时间内反应速率v(CH3OH) = mol-1·(Lmin)-1。 (4)生产过程中,合成气要进行循环,其目的是 。 |
参考解答
⑴①此反应的化学平衡常数表达式为,K=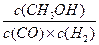 ; ;②BC ⑵Z,催化效率高且活性温度低(或催化活性高速度快,反应温度低产率高) (3)①>。 ②0.03 mol·L-1·min-1。(3分) (4)提高原料利用率(或提高产量、产率亦可)。 |
| 略 |
相似问题
(8分)(1)乙醇的分子结构如右图:其中①②③④⑤表示化学键的代号 用代号回答:i乙醇与钠反应断裂的
(8分)(1)乙醇的分子结构如右图:其中①②③④⑤表示化学键的代号,用代号回答:i乙醇与钠反应断裂的键是_;ii乙醇与氧气在铜或银作催化剂,加热条件
分子式为C5H12O的一元醇有多种同分异构体 其中主链上碳原子数为3的同分异构体数目为m 主链上碳原
分子式为C5H12O的一元醇有多种同分异构体,其中主链上碳原子数为3的同分异构体数目为m,主链上碳原子数目为4的同分异构体数目为n。下列关于m、n的数值正
有两种饱和一元醇的混合物2.293 g与足量的Na充分反应 生成的氢气在标准状况下的体积为560 m
有两种饱和一元醇的混合物2 293 g与足量的Na充分反应,生成的氢气在标准状况下的体积为560 mL,这两种醇分子中相差一个碳原子。则这两种醇是( )A.
燃烧物质的量相等的某有机物和乙醇 实验测得:①乙醇燃烧生成的CO2的量是该有机物燃烧生成的CO2的量
燃烧物质的量相等的某有机物和乙醇,实验测得:①乙醇燃烧生成的CO2的量是该有机物燃烧生成的CO2的量的2 3;②该有机物燃烧生成水的量是乙醇燃烧生成水的
乙醇分子中不同的化学键如图所示 乙醇各种反应中应断裂的键说明不正确的是( )A.和金属钠作用时 键①
乙醇分子中不同的化学键如图所示,乙醇各种反应中应断裂的键说明不正确的是()A.和金属钠作用时,键①断裂B.和浓H2SO4共热至170℃时,键②和⑤断裂C.












