甲 乙 丙 丁 戊为原子序数依次增大的短周期元素.甲 丙处于同一主族 丙 丁 戊处于同一周期 戊原子
| 甲、乙、丙、丁、戊为原子序数依次增大的短周期元素.甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和.甲、乙组成的成见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L也能与Z的水溶液反应生成盐;丙、戊可组成化合物M. 请回答下列问题: (1)戊离子的结构示意图为______. (2)写出乙的单质的电子式:______. (3)戊的单质与X反应生成的Y和Z的物质的量之比为2:4,反应中被氧化的物质与被还原的物质的物质的量之比为______. (4)写出少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:______. (5)按右图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:______.将充分电解后所得溶液逐滴加入到酚酞试液中,观察到得现象是______. 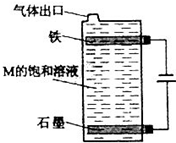 |
参考解答
| 甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝,则X是NH3,甲是H,乙是N,甲、丙处于同一主族,并且丙的原子序数大于N,则丙是Na.根据戊原子的最外层电子数是甲、乙、丙原子的最外层电子数之和,则戊原子最外层电子数=1+1+5=7,则戊是Cl,戊的单质是Cl2,与NH3反应生成乙的单质N2和NH4Cl、HCl;并且0.1 mol?L-1的Y溶液的pH>1,则Y是NH4Cl, Z是HCl,丁的单质能与NaOH溶液反应,也能与HCl水溶液反应,则丁是Na,生成的盐L是NaAlO2,丙、戊组成的化合物M为NaCl; (1)Cl-的结构示意图为: 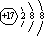 ,故答案为: 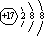 ; (2)乙单质N2中含有共价三键,电子式为: 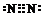 ,故答案为: 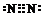 ; (3)NH3与Cl2反应的化学方程式:4NH3+3Cl2═N2+2NH4Cl+4HCl,在反应中氨气做还原剂,氯气做氧化剂,被氧化的物质氨气只占反应掉的一半,被氧化的物质氨气与被还原的物质氯气物质的量之比为:2:3,故答案为:2:3. (4)将少量的盐酸滴入过量NaAlO2溶液中发生反应的离子方程式为:AlO2-+H++H2O═Al(OH)3↓,故答案为:AlO2-+H++H2O═Al(OH)3↓; (5)电解饱和氯化钠溶液,反应的方程式为:2NaCl+2H2O
|
相似问题
下列反应中氯元素被氧化的是( )A.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H
下列反应中氯元素被氧化的是( )A.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2OB.5Cl2+I2+6H2O=10HCl+2HIO3C.2NaCl+2H2O电解 2NaOH+Cl2↑+H2↑D.MnO2+4HCl=MnCl2+2H2O+Cl2
科学家发现了如下反应:O2+PtF6=O2 (PtF6) O2(PtF6)为离子化合物 其中Pt为+
科学家发现了如下反应:O2+PtF6=O2(PtF6),O2(PtF6)为离子化合物,其中Pt为+5价.下列说法正确的是( )A.O2(PtF6)中不存在共价键B.O2(PtF6
在NO2与水的反应中 NO2( )A.只是氧化剂B.只是还原剂C.既是氧化剂 又是还原剂D.既不是
在NO2与水的反应中,NO2( )A.只是氧化剂B.只是还原剂C.既是氧化剂,又是还原剂D.既不是氧化剂,又不是还原剂
下列变化一定需要加入还原剂才能实现的是( )A.KMnO4→MnO2B.Cl-→Cl2C.H2S→
下列变化一定需要加入还原剂才能实现的是( )A.KMnO4→MnO2B.Cl-→Cl2C.H2S→SO2D.Fe2+→Fe
下列反应属于氧化还原反应 但水既不作氧化剂也不作还原剂的是( )A.CO2+H2O=H2CO3B.
下列反应属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )A.CO2+H2O=H2CO3B.2F2+2H2O=4HF+O2C.Cl2+H2O=HCl+HClOD.2Na+2H2O=2NaOH+H2↑












