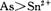某工厂的酸性废水中含有剧毒的可加入除去并回收As 反应的离子方程式为: 下列关于该反应的说法中正确的
某工厂的酸性废水中含有剧毒的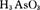 可加入 可加入 除去 除去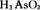 并回收As,反应的离子方程式为: 并回收As,反应的离子方程式为: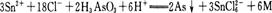 ,下列关于该反应的说法中正确的是( ) ,下列关于该反应的说法中正确的是( )
|
参考解答
| D |
根据物质所含元素的化合价变化可知,在反应中还原剂为Sn2+,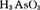 是氧化剂,还原性:Sn2+>As,故A、B不正确;由质量守恒定律可知M为H2O,故C不正确。 是氧化剂,还原性:Sn2+>As,故A、B不正确;由质量守恒定律可知M为H2O,故C不正确。 |
相似问题
已知反应3Cl2+6NaOH(浓)5NaCl+NaClO3+3H2O 下列有关说法正确的是 (
已知反应3Cl2+6NaOH(浓)5NaCl+NaClO3+3H2O,下列有关说法正确的是 ()A.得电子的氯原子数是失电子氯原子数目的6倍B.被氧
已知:异氰酸(HCNO)结构式为H—N=C=O 其中氮元素为-3价.HCNO能和NO2反应生成N2
已知:异氰酸(HCNO)结构式为H—N=C=O,其中氮元素为-3价.HCNO能和NO2反应生成N2、CO2、H2O 下列说法正确的是[]A.在反应中,HCNO既被氧化又被还原 B
IBr的化学性质与卤素单质相似 能与大多数金属反应生成金属卤化物 也可与水发生如下反应:IBr+H2
IBr的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,也可与水发生如下反应:IBr+H2O=HIO+HBr,下列说法正确的是 [ ]A.IBr与Ca(OH)2反应
对于反应3Cl2+6NaOH ==5NaCl+NaClO3+3H2O 以下叙述不正确的是[
对于反应3Cl2+6NaOH==5NaCl+NaClO3+3H2O,以下叙述不正确的是[ ]A.NaClO3中Cl的化合价是+5 B.被氧化的Cl原子和被还原的Cl原子的物质的量的比为1∶5
废水中常含有卤代烃 研究发现 把铁粉放在废水中可以除去卤代烃 该过程的机理为:Fe+ RCH2X+
废水中常含有卤代烃,研究发现,把铁粉放在废水中可以除去卤代烃,该过程的机理为:Fe+ RCH2X+ H+ →RCH3+X-+Fe2+(X 为卤素)。下列说法中正确的是[