在反应3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O中 当有1 mol铜被氧化
在反应3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O中,当有1 mol铜被氧化时,被还原的硝酸为( )
|
参考解答
| D |
试题分析:根据方程式可知,每消耗3mol铜,生成2molNO,这说明被还原的硝酸是2mol。所以当有1 mol铜被氧化时,被还原的硝酸的物质的量是 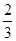 mol,答案选D。 mol,答案选D。点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养。该题的关键是明确氧化还原反应的有关概念,然后结合题意灵活运用即可,有利于培养学生的逻辑推理能力和规范的答题能力。 |
相似问题
(1)粗盐中常含有泥沙和Ca2+ Mg2+ Fe3+ SO2-4等杂质 必须精制后才能供电解使用。精
(1)粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO2-4等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②H
下列反应中有关电子转移的数目分析正确的是A.某密闭容器盛有2molN2和6molH2 在一定条件下充
下列反应中有关电子转移的数目分析正确的是A.某密闭容器盛有2molN2和6molH2,在一定条件下充分反应,转移电子的数目为12NAB.标准状况下,1molCl2溶于水
高锰酸钾(KMnO4)是一种常用的氧化剂。(1)有下列变化:CO32-→CO2 C2O42-→CO2
高锰酸钾(KMnO4)是一种常用的氧化剂。(1)有下列变化:CO32-→CO2、C2O42-→CO2、Fe3+→Fe2+,找出其中一个变化与“MnO4-→Mn2+”组成一个反应,写出
据报道 人工光合作用能够借助太阳能 用CO2和H2O制备HCOOH 其反应原理如下:2CO2+2H2
据报道,人工光合作用能够借助太阳能,用CO2和H2O制备HCOOH,其反应原理如下:2CO2+2H2O 2HCOOH+O2,下列说法正确的是A.HCOOH分子中含有极性键,又有非
已知A2On2-可与B2-反应 B2-被氧化 产物为B单质 A2On2-被还原 产物为A3+;且知1
已知A2On2-可与B2-反应,B2-被氧化,产物为B单质,A2On2-被还原,产物为A3+;且知100mL c(A2On2-)=0 3mol L的溶液与150mL c(B2-)="0 " 6mol L的


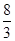 mol
mol









