现有含淀粉 NaCl Na2SO4 CaCl2的混合溶液 选择适当的试剂和方法从中提纯出NaCl晶体
现有含淀粉、NaCl、Na2SO4、CaCl2的混合溶液,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下: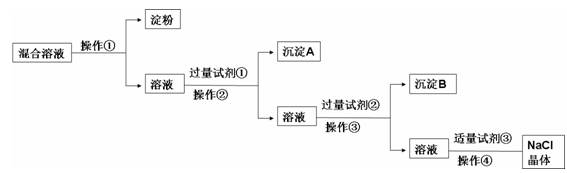 (1)a.操作①是利用胶体中胶体粒子______________(填“能”或“不能”)透过半透膜,溶液溶质分子、离子__________(填“能”或“不能”)透过半透膜进行分离提纯。 b.如何用实验证明淀粉未透过半透膜而Cl-已透过半透膜: ______________________________________________________ _____________ ______ (2)写出上述实验过程中所用试剂: 试剂①_______________________;试剂③________________________。 (3)判断试剂①已过量的方法是:________________________________________。 (4)用化学方程式表示加入试剂②的作用: ________________________________________________________ ____________ (5)操作④的名称是__________________________。 |
参考解答
| (1)a.不能; 能; b.用两支试管分别取半透膜外的溶液,往其中一支试管滴加AgNO3溶液,产生白色沉淀,说明Cl-已透过半透膜;往另一支试管滴加碘水,溶液不变蓝,说明淀粉未透过半透膜。 (2)氯化钡溶液;稀盐酸 (3)静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量。 (4)BaCl2+Na2CO3=2NaCl+BaCO3↓ CaCl2+Na2CO3=2NaCl+CaCO3↓ (5)蒸发(结晶) |
| 略 |
相似问题
能正确表示下列反应的离子方程式是( )A.将Fe(OH)3溶于HI溶液中:Fe(OH)3+
能正确表示下列反应的离子方程式是()A.将Fe(OH)3溶于HI溶液中:Fe(OH)3+3H+=Fe3++3H2O B.NaHCO3溶液水解:HCO3-+H2O CO32-+H3O+C.用浓硫酸酸化
下列离子方程式表达正确的是( )A.用惰性电极电解熔融氯化钠:2Cl-+2H2OCl2↑+H2
下列离子方程式表达正确的是()A.用惰性电极电解熔融氯化钠:2Cl-+2H2OCl2↑+H2↑+2OH-B.用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-=2AlO2
(6分)有一瓶澄清的溶液 其中可能含NH4+ K+ Na + Mg2+ Ba2+ Al3+ Fe
(6分)有一瓶澄清的溶液,其中可能含NH4+、K+、Na +、Mg2+、Ba2+、 Al3+、 Fe3+、SO42-、CO32-、NO3-、Cl-、I-,取该溶液进行如下实验:
下列离子方程式的书写正确的是A.碳酸钙溶于醋酸中:CaCO3+2H+══Ca2++H2O+CO2↑B
下列离子方程式的书写正确的是A.碳酸钙溶于醋酸中:CaCO3+2H+══Ca2++H2O+CO2↑B.钠与水反应:Na + 2H2O ══Na+ + H 2↑+ 2OH-C.在CuSO
只选用一种试剂鉴别NaNO3 Ba(HCO3)2 BaCl2 Na2CO3四瓶无色溶液 应选用
只选用一种试剂鉴别NaNO3、Ba(HCO3)2、BaCl2、Na2CO3四瓶无色溶液,应选用 做试剂,有关的离子方程式是⑴⑵⑶












