配平下列化学方程式:(1)K2Cr2O7+HCl(浓)——KCl+CrCl3+Cl2↑+H2O(2)
| 配平下列化学方程式: (1)K2Cr2O7+HCl(浓)——KCl+CrCl3+Cl2↑+H2O (2)Fe3C+HNO3(浓)——Fe(NO3)3+CO2↑+NO2↑+H2O (3)Fe(OH)3+NaOH+Cl2——Na2FeO4+NaCl+H2O (4)S+Ca(OH)2——CaSx+CaS2O3+H2O (5) 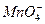 +H2S+H+——Mn2++S↓+H2O +H2S+H+——Mn2++S↓+H2O |
参考解答
| (1)K2Cr2O7+14HCl(浓)====2KCl+2CrCl3+3Cl2↑+7H2O (2)Fe3C+22HNO3(浓)====3Fe(NO3)3+CO2↑+13NO2↑+11H2O (3)2Fe(OH)3+10NaOH+3Cl2====2Na2FeO4+6NaCl+8H2O (4)2(x+1)S+3Ca(OH)2====2CaSx+CaS2O3+3H2O (5)2 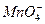 +5H2S+6H+====2Mn2++5S↓+8H2O +5H2S+6H+====2Mn2++5S↓+8H2O |
(1)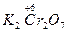 +H +H 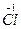 (浓)——KCl+ (浓)——KCl+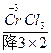 + +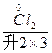 +H2O +H2O首s先确定CrCl3和Cl2的化学计量数分别是2和3,然后根据反应前后各种原子个数相等配平得:K2Cr2O7+14HCl(浓)====2KCl+2CrCl3+3Cl2↑+7H2O 逆配法:部分氧化还原反应、自身氧化还原反应、歧化反应等宜选用此种方法配平,即先从氧化产物和还原产物开始配平。 (2) 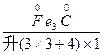 + +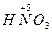 (浓)—— (浓)——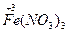 + +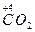 ↑+ ↑+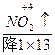 +H2O +H2O首先确定Fe3C和NO2的化学计量数分别是1和13,然后根据反应前后各种原子个数相等配平得:Fe3C+22HNO3(浓)====3Fe(NO3)3+CO2↑+13NO2↑+11H2O 零价法:对于不易确定元素化合价的物质(如铁、砷、碳等组成的化合物)参加的氧化还原反应,根据化合物中各元素的化合价代数和为零的原则,把组成该物质的各元素化合价看作零价,然后计算出各元素化合价的升降值,并使升降值相等。 (3)反应物中H∶O=1∶1,则Na2FeO4∶H2O=1∶4,设Na2FeO4的化学计量数为1,则H2O的化学计量数为4,根据反应前后各种原子个数相等配平得: 2Fe(OH)3+10NaOH+3Cl2====2Na2FeO4+6NaCl+8H2O 定组成法:对一个确定的化合物而言,各组成元素的原子个数之比一定,由此决定了反应物或生成物中可能有两种或两种以上的物质的比例关系一定,据此可实现配平。 (4)S0+Ca(OH)2—— 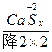 + +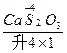 +H2O +H2O首先确定CaSx和CaS2O3的化学计量数分别是2和1,然后根据反应前后各种原子个数相等配平得:2(x+1)S+3Ca(OH)2====2CaSx+CaS2O3+3H2O 整体标价法:当化合物中某一元素有多个(或为不定数)时,可将它作为整体,计算其整体的化合价。 (5)第一步,根据得失电子守恒配平 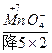 + +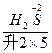 +H+——Mn2++ +H+——Mn2++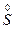 ↓+H2O ↓+H2O则2 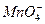 +5H2S+H+——2Mn2++5S↓+H2O +5H2S+H+——2Mn2++5S↓+H2O第二步,根据电荷守恒,两边离子电荷相等需要6个H+来配平,则:2 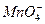 +5H2S+6H+——2Mn2++5S↓+H2O +5H2S+6H+——2Mn2++5S↓+H2O第三步,根据质量守恒配平得:2 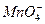 +5H2S+6H+====2Mn2++5S↓+8H2O +5H2S+6H+====2Mn2++5S↓+8H2O氧化还原型离子方程式的配平法:离子方程式的配平依据是得失电子守恒、电荷守恒和质量守恒,即首先根据得失电子守恒配平氧化剂、还原剂、氧化产物、还原产物的化学计量数,在此基础上根据电荷守恒,配平两边离子所带电荷数,最后根据质量守恒配平其余物质的化学计量数。 |
相似问题
下列说法正确的是( )A.Ksp反映了物质在水中的溶解能力 但不可以直接根据Ksp的数值大小比较
下列说法正确的是()A.Ksp反映了物质在水中的溶解能力,但不可以直接根据Ksp的数值大小比较电解质在水中的溶解能力大小B.乙醇汽油是多种烃的混合物C.
某温度(t℃)时 水的Kw=1×10-12 则该温度(填“>” “
某温度(t℃)时,水的Kw=1×10-12,则该温度(填“>”、“<”或“=”)25℃,其理由是。⑴将此温度下pH=11的NaOH与pH="1" HCl等体积混合,混合后溶液p
下列各组离子 在指定环境中能大量共存的是( )A.常温下 在PH=1的溶液:Cu2+ Na+ Mg
下列各组离子,在指定环境中能大量共存的是( )A.常温下,在PH=1的溶液:Cu2+、Na+、Mg2+、NO3-B.常温下,在滴加酚酞试液显红色的溶液:K+、HCO3-
某溶液中存在较多的H+ SO42- Cl- 该溶液中还可能大量存在的离子是( )A.OH-B.Ba
某溶液中存在较多的H+、SO42-、Cl-,该溶液中还可能大量存在的离子是( )A.OH-B.Ba2+C.NH4+D.Ag+
下列各种溶液中 能大量共存的无色透明的离子组( )A.PH=0的溶液:Fe2+ NO3- SO42
下列各种溶液中,能大量共存的无色透明的离子组( )A.PH=0的溶液:Fe2+、NO3-、SO42-、I-B.C(H+)=10-14mol?L-1的溶液中:Na+、[Al(OH)4]-、S2-












