海水是一种丰富的资源 工业上从海水中可提取许多种物质 广泛应用于生活 生产 科技等方面。下图是某工厂
海水是一种丰富的资源,工业上从海水中可提取许多种物质,广泛应用于生活、生产、科技等方面。下图是某工厂对海水资源进行综合利用的示意图。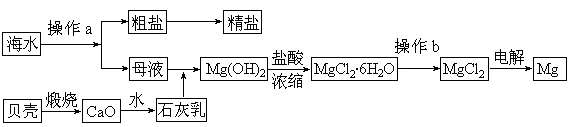 回答下列问题: (1)流程图中操作a的名称为 。 (2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。 ①已知气体A、B是CO2或NH3,则气体A应是 (填化学式)。 ②灼烧晶体C的反应方程式为 。 ③滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却后,可析出不含有NaHCO3的副产品NH4Cl晶体,则通入NH3的作用是 。 (3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。 ① 若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是: 。 ② 通过操作b获得无水MgCl2是在 氛围中进行,若直接在空气中加热,则会生成Mg(OH)Cl,写出有关反应的化学方程式: 。 |
参考解答
| (1)蒸发结晶(或蒸发)………(2分) (2)①NH3……(2分) ②2NaHCO3  Na2CO3+CO2↑+H2O……… (2分) Na2CO3+CO2↑+H2O……… (2分)③增加NH4+的浓度,有利于沉淀平衡向生成NH4Cl的方向进行,并将NaHCO3转化为Na2CO3而不析出。………(两点各1分,共2分) (3)①用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色火焰产生,则证明所得无水氯化镁晶体中不含氯化钠。………(2分)(或答焰色反应也给分) ②HCl(气流)……(2分) MgCl2·6H2O  Mg(OH)Cl+HCl↑+5H2O↑……(2分) Mg(OH)Cl+HCl↑+5H2O↑……(2分) |
试题分析:(1)由流程图可知是从海水中分离出粗盐,即从溶液中分离出溶质,故用蒸发结晶的方法。 (2)①由于二氧化碳在水中的溶解度很小,而氨气极易溶于水,溶液显碱性,所以制取碳酸氢钠的方法是向饱和的氯化钠溶液中依次通入氨气、二氧化碳,析出碳酸氢钠晶体,加热碳酸氢钠晶体可制得纯碱,因此A是氨气。 ②C是碳酸氢钠,不稳定加热易分解生成碳酸钠、二氧化碳和水,所以灼烧晶体C的反应方程式为2NaHCO3  Na2CO3+CO2↑+H2O。 Na2CO3+CO2↑+H2O。③由于氨气溶于水后生成氨水,氨水电离成铵根和氢氧根离子,增大铵根的浓度有利于氯化铵的析出,所以通入氨气的作用是增加NH4+的浓度,有利于沉淀平衡向生成NH4Cl的方向进行,并将NaHCO3转化为Na2CO3而不析出。 (3)①要验证所得无水MgCl2中不含NaCl,最简单的操作方法是焰色反应,即用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色火焰产生,则证明所得无水氯化镁晶体中不含氯化钠。 ②如果直接在空气中加热MgCl2?6H2O,则Mg2+会水解的生成Mg(OH)Cl和HCl,通入HCl可以抑制其水解;其反应方程式为MgCl2·6H2O  Mg(OH)Cl+HCl↑+5H2O↑。 Mg(OH)Cl+HCl↑+5H2O↑。 |
相似问题
下列有关钠及其化合物的说法中正确的是( )A.在Na2SO4 Na2O以及Na2O2中 阳离子与阴
下列有关钠及其化合物的说法中正确的是()A.在Na2SO4、Na2O以及Na2O2中,阳离子与阴离子的个数比均为2∶1B.实验桌上金属钠着火不能用常规灭火器灭火,
下列有关钠的叙述中 正确的是 [ ]A.钠的质地软 可用小刀切割 B.钠是一种灰黑色的固体
下列有关钠的叙述中,正确的是 [ ]A.钠的质地软,可用小刀切割 B.钠是一种灰黑色的固体 C.钠的化学性质非常活泼,在自然界钠可以以化合态和游离态
足量的二氧化碳通入到1mol/L NaOH溶液中 下列说法错误的是A.溶液中Na+离子个数为NA(N
足量的二氧化碳通入到1mol L NaOH溶液中,下列说法错误的是A.溶液中Na+离子个数为NA(NA表示阿伏加德罗常数)B.溶液中的CO32—离子浓度先增大后减小C
把一小块金属钠投入水中 观察到以下各种现象:钠浮在水面上 熔成闪亮的小球 四处游动 逐渐减少 直至消
把一小块金属钠投入水中,观察到以下各种现象:钠浮在水面上,熔成闪亮的小球,四处游动,逐渐减少,直至消失。(1)写出该反应的离子方程式____________
一定温度下 向饱和NaOH溶液中投入一小块金属钠 充分反应后恢复到原来温度。下列叙述中 不合理的是[
一定温度下,向饱和NaOH溶液中投入一小块金属钠,充分反应后恢复到原来温度。下列叙述中,不合理的是[ ]A.NaOH溶液浓度增大,并放出H2 B.溶液中NaOH












