下图是实验室制取气体的常用装置。(1)写出标有序号的仪器名称:① ;②
下图是实验室制取气体的常用装置。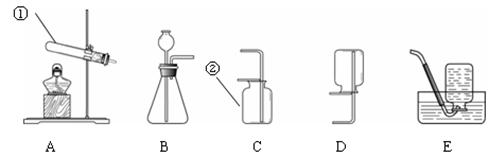 (1)写出标有序号的仪器名称:① ;② 。 (2)用高锰酸钾制取氧气的化学方程式为 ; 实验时应在试管口放一团棉花,其作用是 ; 用排水法收集氧气的合适时机是 。 实验结束时,发现试管破裂,可能原因是: ①实验前忘记检查装置的气密性; ②加热前试管外壁有水珠; ③加热时试管底部触及灯芯; ④试管口向上倾斜; ⑤实验结束时,先熄灭了酒精灯后将导管移出水槽; ⑥没有进行预热,直接对准试管里固体进行加热。其中与之相关的是
该反应原理是(用化学方程式表示) |
参考解答
| 试管、集气瓶 2KMnO4△K2MnO4 + MnO2 + O2↑ 防止加热时高锰酸钾粉末进入导管 当气泡均匀连续冒出时; C BC、 固体和液体反应且不需加热 CaCO3+2HCl=CaCl2+H2O+CO2↑ |
试题分析:(1)熟悉常见仪器,了解其名称,图中①是试管;②是集气瓶; (2)加热高锰酸钾分解制取氧气的同时,还生成了锰酸钾、二氧化锰,故反应的化学方程式是2KMnO4 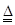 K2MnO4+MnO2+O2↑; K2MnO4+MnO2+O2↑;由于高锰酸钾粉末在加热时,会随氧气流进入导管,故要在试管口加一团棉花加以阻挡; 由于试管中本身存在有一定量的空气,所以要先将空气排尽后才能收集氧气,一般等到气泡均匀连续冒出时即可收集; 造成试管炸裂原因,主要是受热不均匀引起的。 ①实验前忘记检查装置的气密性,有可能会漏气,但试管不会破裂; ②加热前试管外壁有水珠,由于水分蒸发吸热,造成各部分受热不均匀而破裂; ③加热时试管底部触及灯芯,由于火焰的各部温度不同,会造成试管受热不均匀而破裂; ④试管口向上倾斜,管口会有冷凝水回流,使试管炸裂; ⑤实验结束时,先熄灭了酒精灯后将导管移出水槽,会导致水槽中的水倒吸进入试管,使试管炸裂; ⑥没有进行预热,直接对准试管里固体进行加热,会造成局部受热过高,即受热不均匀而破裂。故选C (3)制取气体的装置分为发生装置和收集装置,发生装置的选择,需要考虑反应物的状态和反应条件;收集装置的选择,需要考虑生成气体的水溶性和密度与空气的大小。实验室一般用大理石(主要成分是碳酸钙)和稀盐酸反应制取二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;由于使用的是固体和液体反应,且不需加热,故发生装置可选B装置;由于二氧化碳的密度比空气大,能够溶于水,所以只能用向上排空气法收集,故用C装置来收集。 点评:常见气体的发生装置,依据反应物的状态和反应条件,可分为“固体加热型”和“固液常温型”两种装置;常用气体的收集装置,依据气体的溶解性、密度及其是否与水或者空气的成分发生反应,可分为“排水法”、“向下排空气法”、“向上排空气法”三种装置来收集。 |
相似问题
某气体即能用向上排空气法收集 又能用排水法收集的是A.易溶于水 密度比空气大B.易溶于水 密度比空气
某气体即能用向上排空气法收集,又能用排水法收集的是A.易溶于水,密度比空气大B.易溶于水,密度比空气小C.难溶于水,密度比空气小D.难溶于水,密度
(5分)写出下列反应的文字表达式 并标明基本反应类型(1)铁丝在氧气中燃烧
(5分)写出下列反应的文字表达式,并标明基本反应类型(1)铁丝在氧气中燃烧();(2)加热高锰酸钾制氧气();(3)高温下碳与氧化铜反应生成铜和二
(11分)请你根据下图提供的氧气的制取和性质实验 回答以下问题。(1)指出图中标有a和b的仪器名称:
(11分)请你根据下图提供的氧气的制取和性质实验,回答以下问题。(1)指出图中标有a和b的仪器名称:a、 b。(2)根据图A中观察到的现象,说明该反应生
(10分):根据右列装置图回答问题(1)写出图中标号的仪器称:a b
(10分):根据右列装置图回答问题(1)写出图中标号的仪器称:ab cd e f (2)请用A、B、C、D、E填空: 制取二氧化碳选用,收集CO2选择。(3)请
(9分)通过半个学期的化学学习 你已经掌握了实验室制取气体的有关基础知识 请结合下列装置图 回答问题
(9分)通过半个学期的化学学习,你已经掌握了实验室制取气体的有关基础知识,请结合下列装置图,回答问题:⑴ 写出用高锰酸钾来制取氧气的文字表式。⑵












