已知:①CO(g)+H2O(g)CO2(g)+H2(g) ΔH1='-41.2' kJ/mol②C
已知:①CO(g)+H2O(g) CO2(g)+H2(g) ΔH1="-41.2" kJ/mol CO2(g)+H2(g) ΔH1="-41.2" kJ/mol②CH4(g)+CO2(g)  2CO(g)+2H2(g) ΔH2="+247.3" kJ/mol 2CO(g)+2H2(g) ΔH2="+247.3" kJ/mol③CH4(g)+H2O(g)  CO(g)+3H2(g) ΔH3 CO(g)+3H2(g) ΔH3若反应③在一体积恒定为1 L的密闭容器中进行,测得CH4的物质的量浓度随反应时间的变化如图所示。下列有关叙述错误的是 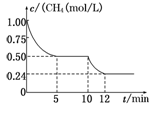
|
参考解答
| D |
| A、正确,①+②得△H3=-41.2 kJ/mol+247.3 kJ/mol=+206.1 kJ/mol B、正确,升高温度,平衡正向移动;C、正确,206.1 kJ/mol×0.5mol='103.05' kJ;D、不正确,CH4的转化率将减小。选D。 |
相似问题
向某密闭容器中充入1 mol CO和2 mol H2O(g) 发生反应:CO(g)+H2O(g)CO
向某密闭容器中充入1 mol CO和2 mol H2O(g),发生反应:CO(g)+H2O(g)CO2(g)+H2(g)。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不
二氧化硫与氧气的反应为:2SO2(g)+ O2(g) 2 SO3 (g); △H
二氧化硫与氧气的反应为:2SO2(g)+ O2(g) 2 SO3 (g); △H <0, 该反应在硫酸工业生产中应采取的适宜条件是()A.低温、高压、催化剂B.适宜的温
在气相条件下(T='500' K) 有相同体积的甲 乙两容器 甲容器充入1 g SO2 l gO2
在气相条件下(T="500" K),有相同体积的甲、乙两容器,甲容器充入1 g SO2、l gO2,乙容器充入2 g SO2、2g O2则下列叙述中正确的是A.化学反应速率
在一定体积的密闭容器中 进行反应CO2(g)+ H2(g) CO(g)+ H2O(g)。其平衡常数K
在一定体积的密闭容器中,进行反应CO2(g)+ H2(g) CO(g)+ H2O(g)。其平衡常数K和温度T的关系如表所示:T ℃70080083010001200K0 60 91 01 72 6回答下列
如图所示 当关闭K时 向A 中充入2molX 7molY 向B中充入4molX 14molY 起始时
如图所示,当关闭K时,向A 中充入2molX、7molY,向B中充入4molX、14molY,起始时VA=VB=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应












