某温度下 反应 2CH3OH(g) CH3OCH3(g) + H2O(g)的平衡常数为400。此温
某温度下,反应 2CH3OH(g) 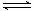 CH3OCH3(g) + H2O(g)的平衡常数为400。此温度下,在容积一定的密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下: CH3OCH3(g) + H2O(g)的平衡常数为400。此温度下,在容积一定的密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
A.CH3OH的起始浓度为1.04 mol/L B.此时逆反应速率大于正反应速率 C.平衡时,CH3OH的浓度为0.04 mol/L D.平衡时,CH3OH的转化率小于80% |
参考解答
| C |
| 由表格中数据可求得甲醇的起始浓度为 反应 2CH3OH(g) 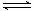 CH3OCH3(g) + H2O(g) CH3OCH3(g) + H2O(g)起始浓度: 1.64 0 0 转化浓度: 1.2 0.6 0.6 该时刻浓度:0.44 0.6 0.6 平衡时: 由表格所给数据可求得: 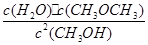 = =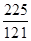 <400,故反应将正向进行,正反应速率大于逆反应速率; <400,故反应将正向进行,正反应速率大于逆反应速率;而平衡时各物质浓度: 反应 2CH3OH(g) 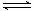 CH3OCH3(g) + H2O(g) CH3OCH3(g) + H2O(g)起始浓度: 1.64 0 0 转化浓度: x x/2 x/2 平衡时: 1.64-x x/2 x/2 代入平衡常数关系式可求得:K= 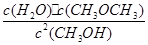 =400,得x为1.6 mol/L,故平衡时CH3OH的浓度为0.04 mol/L,其转化率为 =400,得x为1.6 mol/L,故平衡时CH3OH的浓度为0.04 mol/L,其转化率为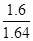 >80% >80%故答案为C |
相似问题
现有带活塞的密闭容器A和B 一定温度时容器A装入碘化氢气体 容器B装入二氧化氮气体 使其体积相等。当
现有带活塞的密闭容器A和B,一定温度时容器A装入碘化氢气体、容器B装入二氧化氮气体,使其体积相等。当温度不变时,缓缓压缩两容器,使两容器的压强均为
将2molA和2molB两种气体混合于2L密闭容器中 发生如下反应: 2分钟末反应达到平衡状态 生成
将2molA和2molB两种气体混合于2L密闭容器中,发生如下反应:,2分钟末反应达到平衡状态,生成了0 8mol D,请填写下面空白:(1)B的平衡浓度为___________
t℃时 将3molA和1molB气体通入体积为2L的密闭容器中(容积不变) 发生如下反应:3A(g)
t℃时,将3molA和1molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g) xC(g)。2min时反应达到平衡状态(温度不变),剩余了0 8m
在其他条件不变的情况下 能使合成氨反应进行程度增大的方法是A.升高温度B.减小压强C.使用催化剂D.
在其他条件不变的情况下,能使合成氨反应进行程度增大的方法是A.升高温度B.减小压强C.使用催化剂D.及时分离出氨气
在某温度下 反应ClF(g)+F2(g) ClF3(g)(正反应为放热反应)在密闭容器中达到平衡。下
在某温度下,反应ClF(g)+F2(g)ClF3(g)(正反应为放热反应)在密闭容器中达到平衡。下列说法正确的是A.温度不变,缩小体积,ClF的转化率增大B.温度不变












