(6分)用VSEPR 理论判断:物质孤对电子对数轨道杂化形式分子或离子的形状NH4+ NCl3
(6分)用VSEPR 理论判断:
|
参考解答
(6分)用VSEPR理论判断:(各1分)
|
由公式:孤对电子对数=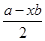 可求得NH4+为0、NCl3为1,价层电子对数分别为4、3,则轨道杂化形式均为Sp3,但微粒形状分别为正四面体和三角锥形。 可求得NH4+为0、NCl3为1,价层电子对数分别为4、3,则轨道杂化形式均为Sp3,但微粒形状分别为正四面体和三角锥形。 |
相似问题
有关CH2=CH-C≡N分子的说法正确的是( )A.3个键 2个π键B.5个键 3个π键 C
有关CH2=CH-C≡N分子的说法正确的是( )A.3个键,2个π键B.5个键,3个π键 C.6个键,2个π键D.6个键,3个π键
下列叙述正确的是( )A.化合物中一定含有σ键 可能含π键B.由非金属元素组成的化合物不一定是共价
下列叙述正确的是( )A.化合物中一定含有σ键,可能含π键B.由非金属元素组成的化合物不一定是共价化合物C.非极性键只存在于单质分子里D.所有原子
关于氢键 下列说法正确的是( )A.氢键比分子间作用力强 所以它属于化学键B.冰中存在氢键
关于氢键,下列说法正确的是()A.氢键比分子间作用力强,所以它属于化学键B.冰中存在氢键,水中不存在氢键C.分子间形成的氢键使物质的熔点和沸点升高
下列物质含有离子键的是A.C12B.NaClC.CO2D.H2O
下列物质含有离子键的是A.C12B.NaClC.CO2D.H2O
(14分)某短周期元素的原子最外层电子数为次外层的2倍 其单质甲可发生如下反应:甲 + 乙丙 + 丁
(14分)某短周期元素的原子最外层电子数为次外层的2倍,其单质甲可发生如下反应:甲 + 乙丙 + 丁 + 水。(1)若丙为NO2。①甲与乙反应的化学方程












