(12分)向20 mL HCl和H2SO4的混合溶液中逐滴加入0.1 mol·L-1的Ba(OH)2
(12分)向20 mL HCl和H2SO4的混合溶液中逐滴加入0.1 mol·L-1的Ba(OH)2溶液,生成沉淀的质量和溶液的pH与加入的Ba(OH)2溶液体积的关系如图5所示。试完成下列问题: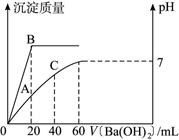 图5 (1)起始时,混合酸中硫酸的物质的量浓度为______________ mol·L-1。 (2)起始时,混合酸中盐酸的物质的量浓度为______________ mol·L-1。 (3)B点表示的沉淀的质量为______________g。 (4)A点表示溶液中的[H+]为______________ mol·L-1,pH为______________。 (5)C点的pH为______________(pH可直接用对数表示)。 |
参考解答
| (1)0.1 (2)0.4 (3)0.466 (4)0.2 07 (5)1.18或-lg 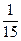 |
Ba2++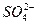 ====BaSO4↓ ====BaSO4↓H+ + OH-====H2O 1 1 1 n( 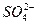 )=n〔Ba(OH)2〕='0.02' L×0.1 mol·L-1=2×10-3 mol )=n〔Ba(OH)2〕='0.02' L×0.1 mol·L-1=2×10-3 mol c(H2SO4)=n(H2SO4)/V(aq)=2×10-3 mol/002 L='0.1' mol·L-1 n(H+)=2×0.06 L×0.1 mol·L-1='0.012' mol n(HCl)=n(H+)-2n(H2SO4)='0.012' mol-2×0.002 mol='0.008' mol c(HCl)='n(HCl)/V(aq)=0.008' mol/0.02 L='0.4' mol·L-1 n(BaSO4)=n( 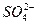 )='0.002' mol )='0.002' molm(BaSO4)=n(BaSO4)·M(BaSO4)='0.002' mol×233 g·mol-1='0.466' g (4)在A点时,Ba(OH)2恰好与H2SO4完全反应,这时溶液中剩余的H+全部是HCl的,n(H+)='n(HCl)=0.008' mol,所以,c(H+)=n(H+)/V(总)='0.008' mol/0.04 L='0.2' mol·L-1,pH='-lg' 0.2=0.7。 (5)C点时的混合液是在A点的基础上又滴入20 mL Ba(OH)2溶液,这时Ba(OH)2只与HCl反应,剩余的H+是n(H+)='0.008' mol-2n〔Ba(OH)2〕='0.008' mol-2×0.1 mol·L-1×0.02 L='0.004' mol,c(H+)='0.004' mol/0.06 L='1/15' mol·L-1。pH=-lg 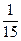 。 。 |
相似问题
(3分)写出以下物质中所含化学键的类型。(1)Cl2_________;(2)NaOH_______
(3分)写出以下物质中所含化学键的类型。(1)Cl2_________;(2)NaOH_________;(3)NaCl________。
下列对分子结构叙述不正确的是( )A.H2O2分子中 两个O之间形成1对共用电子对B.N2的电子
下列对分子结构叙述不正确的是()A.H2O2分子中,两个O之间形成1对共用电子对B.N2的电子式是N┇┇NC.CCl4和甲烷都是正四面体型分子D.CO2和CS2都是直线型分子
两个硫酸分子可以脱去一分子水生成焦硫酸(H2S2O7)。已知硫酸的分子中有4个硫氧键 则焦硫酸分子中
两个硫酸分子可以脱去一分子水生成焦硫酸(H2S2O7)。已知硫酸的分子中有4个硫氧键,则焦硫酸分子中硫氧键的数目是A.4B.6C.7D.8
下列各组物质中化学键类型与晶体类型均相同的是( )A.HCl NaClB.SiO2 CO2C.N
下列各组物质中化学键类型与晶体类型均相同的是()A.HCl NaClB.SiO2 CO2C.Na2CO3 KClO3D.H2O2 Na2O2
通常情况下 能用浓硫酸干燥且属于非极性分子的气体是A.NH3B.H2SC.CO2D.SO2
通常情况下,能用浓硫酸干燥且属于非极性分子的气体是A.NH3B.H2SC.CO2D.SO2












