原子序数依次增大的A B C D E F G七种短周期主族元素 ① B元素的原子最外层电子数是次外层
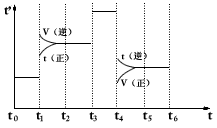
| 原子序数依次增大的A、B、C、D、E、F、G七种短周期主族元素 ① B元素的原子最外层电子数是次外层电子数的两倍, ② C的最高价氧化物的水化物和氢化物反应生成盐 ③ D和E可以形成1:1和1:2的两种常见化合物。 ④ A与C元素原子的电子层数相差1,且与E是同主族元素 ⑤ 原子半径由大到小顺序是E>F>G>B>C>D>A ⑥ F是同周期中离子半径最小的元素,G是同周期中原子半径最小的元素 回答: (1)由B、D、E三元素组成的无机盐水溶液呈碱性,其原因是(用离子方程式表示)_______________________________ (2)A的单质和D的单质可以设计为新型燃料电池,电解质为KOH溶液,则A的单质在该燃料电池中发生的电极反应式为______________________________。 (3)当反应3A2(g)+C2(g) 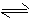 2CA3(g)达到平衡时,不断改变反应条件(不改变A2、C2和CA3的量),下图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是____________________。 2CA3(g)达到平衡时,不断改变反应条件(不改变A2、C2和CA3的量),下图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是____________________。 |
 |
| (4)D和E能形成1:1和1:2的两种常见化合物X和Y :写出Y与水反应的离子方程式:____________________________。若将X、Y分别溶于等量足量的水中,形成浓度相同的溶液,需X、Y的物质的量的关系为:n(X)________n(Y)(填“<”“>”或“=”) (5)C、D、E、F、G的简单离子的半径由大到小的顺序是(用元素的离子符号表示)_____________________________ (6)F的最高价氧化物对应水化物的电离方程式为____________________________ (7)用离子方程式说明C与A形成的化合物结合H+能力强于D与A形成的化合物:____________________ |
参考解答
(1)CO32-+H2O HCO3-+OH- HCO3-+OH- (2)H2+2OH--2e-==2H2O (3)t0-t1 (4)Na2O+H2O==2Na++2OH-;= (5)Cl->N3->O2->Na+>Al3+ (6)Al(OH)3 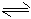 Al3++3OH- Al3++3OH- (7)H3O++NH3==NH4++H2O |
相似问题
A B C均为短周期元素 可形成A2C和BC2两种化合物。A B C的原子序数依次递增 A原子的K层
A、B、C均为短周期元素,可形成A2C和BC2两种化合物。A、B、C的原子序数依次递增,A原子的K层的电子数目只有一个,B位于A的下一周期,它的最外层电子数比K
现有部分短周期元素的性质或原子结构如下表用化学符号回答以下问题:(1)比较:氢化物的稳定性:T___
现有部分短周期元素的性质或原子结构如下表用化学符号回答以下问题:(1)比较:氢化物的稳定性:T_________Z,最高价氧化物对应水化物的酸性:T________
已知四种元素A B C D 为1~20号元素 且原子序数依次增大 A的核外电子数与其电子层数相等;B
已知四种元素A、B、C、D 为1~20号元素,且原子序数依次增大,A的核外电子数与其电子层数相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水
周期表中前四周期中的六种元素A B C D E F原子序数依次增大 已知A原子2p轨道有3个未成对电
周期表中前四周期中的六种元素A、B、C、D、E、F原子序数依次增大,已知A原子2p轨道有3个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两
J L M R T是原子序数依次增大的短周期主族元素 J R在周期表中的相对位置如右表;J元素最低负
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含












