甲醇(CH3OH)是一种重要的化工原料 广泛应用于化工生产 也可以直接用做燃料。已知:CH3OH(1
| 甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用做燃料。已知: CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ;△Ha = -443.64 kJ·mol-1 2CO (g) + O2(g) = 2CO2(g) ;△H b =-566.0 kJ·mol-1 (1)试写出CH3OH(1)在氧气中完全燃烧生成CO2和H2O(g)的热化学方程式:______________________ (2)甲醇作为燃料,它的优点是燃烧时排放的污染物少,从而不仅能缓解能源紧张和温室效应的问题,还能改善大气质量。试利用(1)中的热化学方程式计算,完全燃烧20g甲醇,生成二氧化碳和水蒸汽时,放出的热量为__________kJ,生成的CO2气体标准状况下体积是___________L (3)科研人员新近开发出一种由甲醇和氧气以强碱做电解质溶液的新型手机电池,可使手机连续使用一个月才充一次电,据此回答下列问题: 甲醇在____________极反应;电极反应式为__________________________。 (4)利用电池可实现电能向化学能转化。某同学设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是___________(填序号) |
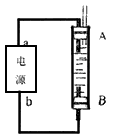 |
| A.电源中的a一定为正极,b一定为负极 B.可以用NaCl溶液作为电解液 C.A、B两端都必须用铁作电极 D.阴极发生的反应是:2H+ + 2e-→H2↑ 若将所得Fe(OH)2沉淀暴露在空气中,其颜色变化是__________________________,反应的化学方程式为 _________________________。 |
参考解答
| (1)2CH3OH(1)+3O2(g)==2CO2(g)+4H2O(g) △H=-1453.28kJ·mol-1 (2)454.15;14 (3)负;CH3OH+8OH--6e-==CO32-+6H2O (4)BD;白色沉淀迅速变成灰绿色,最终变成红褐色;4Fe(OH)2+O2+2H2O==4Fe(OH)3 |
相似问题
最近研发了一种新型的锂空气电池 它既可用作充电电池又可作锂燃料电池。用作燃料电池时 可更换正极的水性
最近研发了一种新型的锂空气电池,它既可用作充电电池又可作锂燃料电池。用作燃料电池时,可更换正极的水性电解液和卡盒以及负极的金属锂就可以连续使用
某电解池内盛有某电解质溶液 插入两根电极 通电后欲达到下列要求:①阳极质量不变②阴极质量增加③电解液
某电解池内盛有某电解质溶液,插入两根电极,通电后欲达到下列要求:①阳极质量不变②阴极质量增加③电解液pH变小。则可选用的电极材料和电解质溶液是[
为使反应:Cu+2H2O===Cu(OH)2+H2↑能够发生 下列设计方案正确的是[ ]A.
为使反应:Cu+2H2O===Cu(OH)2+H2↑能够发生,下列设计方案正确的是[ ]A.用铜片作负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池 B.用铜
下列图示及其解释错误的是[ ]A.图①表示NaCl在水中溶解和电离的示意图B.图②表示碳酸氢
下列图示及其解释错误的是[ ]A.图①表示NaCl在水中溶解和电离的示意图B.图②表示碳酸氢根离子水解示意图 C.符合图③的电离方程式是:HCl+H2O=H3O++C
在水中加入等物质的量的Ag+ Ba2+ SO42- NO3- Cl- Na+ 用惰性材料作电极进行电
在水中加入等物质的量的Ag+、Ba2+、SO42-、NO3-、Cl-、Na+,用惰性材料作电极进行电解,通电片刻后停止,下列说法不正确的是[ ]A.电解的实质是:阳极:












