A.美国《科学》杂志评出的2009年十大科学突破之一是石墨烯的研究和应用方面的突破.石墨烯具有原子级
| A.美国《科学》杂志评出的2009年十大科学突破之一是石墨烯的研究和应用方面的突破.石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构示意图如右: (1)下列有关石墨烯说法正确的是______. A.石墨烯的结构与金刚石相似 B.石墨烯分子中所有原子可以处于同一平面 C.12g石墨烯含σ键数为NA D.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用 (2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合. ①钴原子在基态时,核外电子排布式为:______. 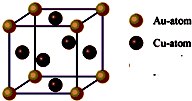 ②乙醇沸点比氯乙烷高,主要原因是______. ③右图是金与铜形成的金属互化物合金,它的化学式可表示为:______. ④含碳源中属于非极性分子的是______(a.甲烷 b.乙炔 c.苯 d.乙醇) ⑤酞菁与酞菁铜染料分子结构如下图,酞菁分子中氮原子采用的杂化方式有:______;酞菁铜分子中心离子的配位数为:______. 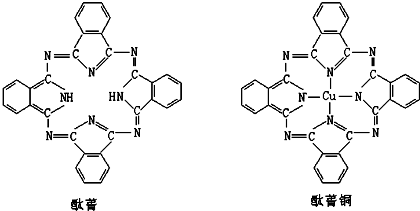 B.硫酸钾是重要的化工产品,生产方法很多,如曼海姆法、石膏两步转化法等. 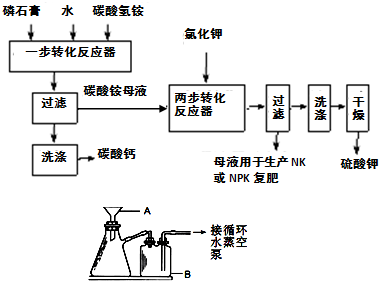 (1)本实验中,采用抽滤方法,图中A、B两仪器名称分别为:______、______. (2)在一部转化反应器中发生的反应为:CaSO4?2H2O+2NH4HCO3=(NH4)2SO4+CaCO3+CO2↑+3H2O,该步反应温度必须低于35℃,其主要目的是____________. (3)在两步转化反应器中发生反应的化学方程式为____________. (4)两步转化反应器中用乙二醇代替水作溶剂,其目的是____________. (5)磷石膏主要成分为二水硫酸钙(CaSO4?2H2O),还含有未分解的磷矿,未洗涤干净的磷酸、氟化钙、铁铝氧化物等,欲检验母液中含Fe3+,可用亚铁氰化钾溶液检验,该检验反应的离子方程式为:______. (6)该法优点除K2SO4产率高外,再列举一个优点____________. 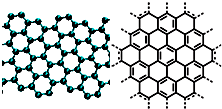 |
参考解答
| (1)A、石墨烯是平面结构,金刚石空间网状结构,故A错误; B.碳碳双键上所有原子都处于同一平面,所以导致石墨烯分子中所有原子可以处于同一平面,故B正确; C.石墨烯中一个碳原子具有1.5个σ键,所以12g石墨烯含σ键数为1.5NA,故C错误; D.石墨结构中,石墨层与层之间存在分子间作用力,所以从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力,故D正确; 故选BD; (2)①钴是27号元素,钴原子核外有27个电子,根据构造原理书写基态原子的核外电子排布式,注意向排4s电子再排3d电子,所以基态钴原子的核外电子排布式为[Ar3d74s2, 故答案为:[Ar3d74s2; ②分子晶体中,物质的熔沸点随着相对分子质量的增大而增大,但乙醇分子间能形成氢键导致乙醇的熔沸点大于氯乙烷的熔沸点, 故答案为:乙醇分子间可形成氢键,而氯乙烷分子间无氢键; ③每个晶胞中含有的铜原子数=6×
④a.甲烷是正四面体结构,属于对称结构,所以是非极性分子; b.乙炔是直线型结构,属于对称结构,所以是非极性分子; c.苯是平面结构,属于对称结构,所以是非极性分子; d.乙醇不是对称结构,所以是极性分子; 故选a、b、c; ⑤酞菁分子中部分氮原子含有2个σ键一个孤对电子,所以采取sp2杂化,部分氮原子含有3个σ键一个孤对电子,所以采取sp3杂化; 该分子中能提供孤对电子的氮原子才是配原子,所以酞菁铜分子中心原子的配位数为:2; 故答案为:sp3和sp2;2; B.(1)A、B两仪器名称分别为:布氏漏斗和安全瓶,故答案为:布氏漏斗;安全瓶; (2)碳酸氢铵易分解,为防止碳酸氢铵分解,所以反应温度必须低于35℃,故答案为:防止NH4HCO3分解; (3)氯化钾和硫酸铵反应生成硫酸钾和氯化铵,反应方程式为:(NH4)2SO4+2KCl=K2SO4+2NH4Cl, 故答案为:(NH4)2SO4+2KCl=K2SO4+2NH4Cl; (4)硫酸钾易溶于水而不易溶于乙二醇,所以加入乙二醇是为了降低K2SO4溶解度,有利于K2SO4析出,提高产率, 故答案为:降低K2SO4溶解度,有利于K2SO4析出,提高产率; (5)铁离子和铁氰化钾反应生成KFe[Fe(CN)6沉淀,其反应方程式为:Fe3++K++[Fe(CN)64-=KFe[Fe(CN)6↓,故答案为:Fe3++K++[Fe(CN)64-=KFe[Fe(CN)6↓; (6)该法优点除K2SO4产率高外,还有原料得到充分利用,同时得到副产品化肥等,故答案为:原料得到充分利用,同时得到副产品化肥等. |
相似问题
下列物质中的原子的杂化轨道类型和分子的立体构型对应有错误的是 [ ]A.BeCl2中的Be
下列物质中的原子的杂化轨道类型和分子的立体构型对应有错误的是 [ ]A.BeCl2中的Be,sp,直线形 B.SiF4中的Si,sp3,正四面体形 C.BCl3中的B,sp2
我国将与德国合作 在近期启动钻探“可燃冰”的实物样品的工作 实现“可燃冰”钻探零的突破.“可燃冰”的
我国将与德国合作,在近期启动钻探“可燃冰”的实物样品的工作,实现“可燃冰”钻探零的突破.“可燃冰”的主要成分是甲烷水合物[CH4?nH2O]晶体.有关甲
下列有机物中含有两个手性碳原子的是[ ]A.B.C.D.
下列有机物中含有两个手性碳原子的是[ ]A.B.C.D.
下列分子中 属于非极性的是( )A.SO2B.BeCl2C.BBr3D.COCl2
下列分子中,属于非极性的是( )A.SO2B.BeCl2C.BBr3D.COCl2
下列有机物中含有两个手性碳原子的是[ ]A. B. C. D.
下列有机物中含有两个手性碳原子的是[ ]A. B. C. D.












