A B C D四种元素位于短周期内 它们的原子序数依次递增。A原子核内仅有1个质子 B原子的电子总数
| A、B、C、D四种元素位于短周期内,它们的原子序数依次递增。A原子核内仅有1个质子,B原子的电子总数与D原子最外层电子数相等,A原子与B原子最外层电子数之和与C原子的最外层电子数相等,D原子与B原子电子总数之和是C原子电子总数的2倍。D原子最外层电子数是其电子层数的3倍。由此推断: (1)A、B、C、D各为什么元素? (2)A与D形成的化合物中,含有非极性键的是________,其电子式为________。 (3)BD2的电子式:________。 |
参考解答
| (1)H C N O (2)H2O2 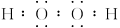 (3) 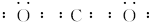 |
因为A原子核内仅有1个质子,所以A为H ;D原子最外层电子数是电子层数的3倍,只能为O ;D原子最外层电子数是电子层数的3倍,只能为O ;B原子的电子总数与D原子最外层电子数相等,B为C ;B原子的电子总数与D原子最外层电子数相等,B为C ;A原子与B原子最外层电子数之和与C最外层电子数相等,C为N ;A原子与B原子最外层电子数之和与C最外层电子数相等,C为N 。 。 |
相似问题
通常状况下 NCl3是一种油状液体 其分子空间构型与氨分子相似 下列对NC13的有关叙述正确的是A.
通常状况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NC13的有关叙述正确的是A.CCl4中C—C1键键长比NC13中N—C1键键长短B.NCl3分子中
在氢 氮 氯和钠四种元素中:(1)有2种元素组成的共价化合物的水溶液显酸性 这种化合物的电子式是
在氢、氮、氯和钠四种元素中:(1)有2种元素组成的共价化合物的水溶液显酸性,这种化合物的电子式是;(2)有2种元素可形成离子化合物,用子电式表示其
SiCl4的分子结构与CCl4类似 对其作出如下判断:①SiCl4晶体是分子组成的晶体 ②常温 常压
SiCl4的分子结构与CCl4类似,对其作出如下判断:①SiCl4晶体是分子组成的晶体②常温、常压下SiCl4是液体③SiCl4的分子是由极性键组成的非极性分子④SiCl4
下列说法中错误的是
下列说法中错误的是()A.键长越短,键能越大,分子越稳定B.分子的性质与键角无关C.分子具有一定的键角,表明共价键具有方向性,由键角可知分子的形状
(7分)根据已有内容的规律进行增补(1)填化学方程式:①2Na+2H2O=2NaOH+H2↑②2HB
(7分)根据已有内容的规律进行增补(1)填化学方程式:①2Na+2H2O=2NaOH+H2↑②2HBr+Cl2=2HCl+Br2[③2H2S+O2=2S+2H2O④_______________________












