已知A B C D E F G H是原子序数依次增大的八种元素 A元素是周期表中原子半径最小的元素
| 已知A、B、C、D、E、F、G、H是原子序数依次增大的八种元素,A元素是周期表中原子半径最小的元素,B、C和D同周期,E、F和G同周期,A、E 同主族,D、G、H同主族且相邻,B的低价氧化物与C单质分子的电子总数相等,F和G的核电荷数相差4,G的2价简单离子与Ar原子的电子层结构相同.根据以上信息填空: (1)G元素的二价离子的离子结构示意图为______;H的元素符号为______,H元素在周期表中的位置是______. (2)C的气态氢化物空间构型是______;A和B形成的四原子非极性分子的结构式是______. (3)据报道,含题中所述元素B、F和Ni三种元素的晶体具有超导性.该晶体的晶胞结构如图,试写出该晶体的化学式______  (4)由A、C、D、G四种元素形成的强酸的酸式盐的水溶液中各离子浓度由大到小的顺序为______. (5)科学家用C、D、E三种元素形成的化合物ECD3和E2D,在573K时反应制得了离子化合物E3CD4;经测定E3CD4中各原子的最外层电子都达到了8电子稳定结构,则CD43-的电子式为______,E3CD4与水能剧烈反应转化为常见物质,写出反应的化学方程式:______. |
参考解答
| A元素是周期表中原子半径最小的元素,故A为H,G的2价简单离子与Ar原子的电子层结构相同,D、G、H同主族且相邻,故G为S,D为O,H为Se,A、E 同主族,则E为Na,B的低价氧化物与C单质分子的电子总数相等,则C为N,B为C,F和G的核电荷数相差4,故F为Mg, (1)硫离子结构示意图为 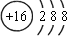 ,H的元素符号为 Se,位于第四周期第ⅥA族,故答案为: 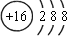 ;Se;第四周期第ⅥA族; (2)氨气的空间结构为三角锥形,碳和氢形成的四原子非极性分子即为乙炔,结构式是:H-C≡C-H,故答案为:三角锥形;H-C≡C-H; (3)根据晶体的晶胞结构,每个晶胞含有一个Mg,含有Ni个数为:6×
(4)硫酸氢铵属于易溶于水的盐,NH4HSO4═NH4++H++SO42-,铵根离子易水解,溶液中的氢离子还有水电离的一小部分,故离子浓度大小顺序为:c(H+)>c(SO42-)>c(NH4+)>c(OH-),故答案为:c(H+)>c(SO42-)>c(NH4+)>c(OH-); (5)NO43-中的化学键全部为共价键,Na3NO4与水反应时,转化为常见物质,根据原子守恒,得到方程式为:Na3NO4+H2O═NaNO3+2NaOH,故答案为: 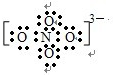 ,Na3NO4+H2O═NaNO3+2NaOH. |
相似问题
原子序数为13的元素位于元素周期表中第______周期 ______族 其原子结构示意图为_____
原子序数为13的元素位于元素周期表中第______周期、______族,其原子结构示意图为______.
画出下列微粒的电子排布图:(1)N _____________ 。 (2)F-___________
画出下列微粒的电子排布图:(1)N _____________ 。 (2)F-______________
某元素原子L层电子数比K层电子数多5个 该元素的最高正价为( )A.+7B.+5C.+3D.无最高
某元素原子L层电子数比K层电子数多5个,该元素的最高正价为( )A.+7B.+5C.+3D.无最高正价
短周期元素A B C D原子序数依次增大 且C元素最高价氧化物对应的水化物 能电离出电子数相等的阴
短周期元素A、B、C、D原子序数依次增大,且C元素最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子.A、C位于同一主族,A为非金属元素,B的最外
已知A B C D E是短周期中的5种非金属元素 它们的原子序数依次增大.A元素原子形成的离子核外电
已知A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大.A元素原子形成的离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子












