根据分子轨道理论解释:在N2和N2+中键长依次为109 pm和112 pm 而在Cl2和Cl2+中键
根据分子轨道理论解释:在N2和N2+中键长依次为109 pm和112 pm,而在Cl2和Cl2+中键长却依次为199 pm和189 pm。
请帮忙给出正确答案和分析,谢谢!
参考解答
正确答案:根据分子轨道理论N2和Cl2的分子轨道分别如下: 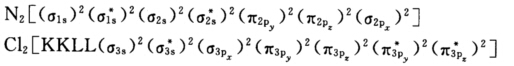 N2的键级为3N2+的键级为2.5;Cl2的键级为1Cl2+的键级为1.5。所以N2的键长比N2+的键长短;而Cl2的键长比Cl2+的键长长。
N2的键级为3N2+的键级为2.5;Cl2的键级为1Cl2+的键级为1.5。所以N2的键长比N2+的键长短;而Cl2的键长比Cl2+的键长长。
根据分子轨道理论,N2和Cl2的分子轨道分别如下:N2的键级为3,N2+的键级为2.5;Cl2的键级为1,Cl2+的键级为1.5。所以N2的键长比N2+的键长短;而Cl2的键长比Cl2+的键长长。
相似问题
判断: (1)化合物的热稳定性GaCl3________________TlCl3; (2)化学活性
判断: (1)化合物的热稳定性GaCl3________________TlCl3; (2)化学活性α-Al2O3________________γ-Al2O3; (3)酸性 Al(OH)3 ________________Ga(OH
用NaH还原四氯化钛请帮忙给出正确答案和分析 谢谢!
用NaH还原四氯化钛请帮忙给出正确答案和分析,谢谢!
硼的卤化物中 只有BF3能发生与HF的加合反应。 ( )此题为判断题(对 错)。请帮忙给出正确答案和
硼的卤化物中,只有BF3能发生与HF的加合反应。 ( )此题为判断题(对,错)。请帮忙给出正确答案和分析,谢谢!
碱金属的熔点 沸点随原子序数增加而降低 因而碱土金属的熔点沸点也会具有这变化规律。 ( )此题为判断
碱金属的熔点、沸点随原子序数增加而降低,因而碱土金属的熔点沸点也会具有这变化规律。 ( )此题为判断题(对,错)。请帮忙给出正确答案和分析,谢谢!
碱金属的氢氧化物都是强碱性的。 ( )此题为判断题(对 错)。请帮忙给出正确答案和分析 谢谢!
碱金属的氢氧化物都是强碱性的。 ( )此题为判断题(对,错)。请帮忙给出正确答案和分析,谢谢!












