t℃时 分别向盛有30克水的两只烧杯中加入等质量的NaCl KNO3两种固体物质 使其充分溶解可观察
t℃时,分别向盛有30克水的两只烧杯中加入等质量的NaCl、KNO3两种固体物质,使其充分溶解可观察到如右图所示的现象,则t℃时______(填“A”或“B”)烧杯中的溶液一定是饱和溶液.50℃时,某溶液所溶解的NaCl和KNO3都已饱和,把该溶液冷却到室温,有晶体析出,经检验发现所析出的晶体主要是KNO3,其原因是______.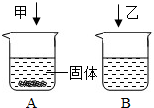 |
参考解答
| 因t℃时,分别向盛有30克水的两只烧杯中加入等质量的NaCl、KNO3两种固体物质, 由图可知,A中有固体不溶解,而B中没有, 根据饱和溶液的概念可知,A中达到了溶解的最大极限, 则A一定是饱和溶液,而B若是恰好完全溶解,则是饱和,即B可能是饱和溶液, 又50℃时,某溶液所溶解的NaCl和KNO3都已饱和,把该溶液冷却到室温,有晶体析出, 根据氯化钠的溶解度受温度的影响变化不大,硝酸钾的溶解度随温度的变化而变化,且变化程度大, 则饱和溶液降温,受温度影响大的固体会从溶液中析出,即析出硝酸钾, 故答案为:A;KNO3的溶解度受温度变化的影响比NaCl大. |
相似问题
如图所示的四个图象表示的变化趋势 分别对应四种操作过程 其中正确的是( )A.某温度下 向一定量接
如图所示的四个图象表示的变化趋势,分别对应四种操作过程,其中正确的是( )A.某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体B.向
炎热的夏天 小林打开冰箱 从4℃的储藏室中拿出一杯内有少量蔗糖晶体的溶液m.在室温下放置一段时间后
炎热的夏天,小林打开冰箱,从4℃的储藏室中拿出一杯内有少量蔗糖晶体的溶液m.在室温下放置一段时间后,发现晶体消失了.得到溶液n.下列说法正确的是(
在一瓶某溶质的饱和溶液中 加入一些该溶质 则( )A.溶质质量减少B.溶质的质量分数增大C.溶质质
在一瓶某溶质的饱和溶液中,加入一些该溶质,则( )A.溶质质量减少B.溶质的质量分数增大C.溶质质量不变D.溶质的溶解度变化
t2℃时 将等质量的a b两种可溶性固体分别加人盛有相同质量水的烧杯中 充分搅拌后的现象如图1所示
t2℃时,将等质量的a、b两种可溶性固体分别加人盛有相同质量水的烧杯中,充分搅拌后的现象如图1所示,a、b两种物质的溶解度曲线如图2所示.请结合图示回
下列说法中 正确的是( )A.饱和溶液一定是浓溶液B.稀溶液一定是不饱和溶液C.固体物质的溶解度
下列说法中,正确的是( )A.饱和溶液一定是浓溶液B.稀溶液一定是不饱和溶液C.固体物质的溶解度,总是随温度降低减少D.某温度下的饱和溶液,改变












