在锌湿法冶炼过程中 会产生大量铜镉渣(主要含有Zn Cd Fe Cu等) 直接丢弃会造成环境污染 也
在锌湿法冶炼过程中,会产生大量铜镉渣(主要含有Zn、Cd、Fe、Cu等),直接丢弃会造成环境污染,也是资源浪费,以下为回收处理铜镉渣制备硫酸锌晶体的工业流程: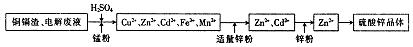 已知:硫酸锌晶体易溶于水,难溶于酒精。 (1)加入硫酸的目的 。 (2)硫酸不能溶出铜,加入锰粉是为了结合铁离子的变价来传递电子,将铜溶出,锰粉的主要成分为MnO2,相关方程式为2Fe3++Cu=2Fe2++Cu2+和 。 (3)由硫酸锌溶液获得硫酸锌晶体,必要的操作方法为 。 (4)制得的硫酸锌晶体需要洗涤,选择的试剂为 ,原因是 。 |
参考解答
| (10分) (1)溶出铜镉渣中的Zn、Cd、Fe等金属(2分) (2) MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O (3分) (3)蒸发浓缩、冷却结晶、过滤(2分) (4)酒精(1分)硫酸锌晶体易溶于水,水洗会造成硫酸锌晶体的损失(2分) |
试题分析: (1)该工艺流程图中可以看出金属单质在硫酸的作用下转变为离子; (2)根据工艺流程图中可以看出溶液中没有Fe2+,且MnO2转变为Mn2+,该反应为氧化还原反应MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O; (3)从溶液中得到晶体的操作; (4)结合题中信息,由于硫酸锌晶体易溶于水,难溶于酒精,应选择酒精洗涤。 |
相似问题
某实验小组对普通锌锰废干电池内的黑色固体进行探究 设计如下方案:己知:I 普通锌锰电池的黑色物质主要
某实验小组对普通锌锰废干电池内的黑色固体进行探究,设计如下方案:己知:I、普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。II、氢氧化锌
已知化合物甲和乙都不溶于水 甲可溶于质量分数大于或等于98%的硫酸 而乙不溶。现有一份甲和乙的混合物
已知化合物甲和乙都不溶于水,甲可溶于质量分数大于或等于98%的硫酸,而乙不溶。现有一份甲和乙的混合物样品,通过实验进行分离,可得到固体甲。(实验中
下列各组溶液 只要用试管和胶头滴管 不用任何化学试剂就可以鉴别的是A.KOH和Al2(SO4)3B.
下列各组溶液,只要用试管和胶头滴管,不用任何化学试剂就可以鉴别的是A.KOH和Al2(SO4)3B.稀H2SO4和NaHCO3C.CaCl2和Na2CO3D.Ba(OH)2和NaHSO4
某无色溶液可能是AgNO3溶液 NaCl溶液 Na2CO3溶液和Na2SO4溶液中的一种。为检验其成
某无色溶液可能是AgNO3溶液、NaCl溶液、Na2CO3溶液和Na2SO4溶液中的一种。为检验其成分,某同学做实验如下:取少量该溶液放入试管中,加入稀盐酸酸化,无
除去CO2中的HCl杂质最好是将混合气体通过足量的A.饱和NaOH溶液B.饱和NaHCO3溶液C.饱
除去CO2中的HCl杂质最好是将混合气体通过足量的A.饱和NaOH溶液B.饱和NaHCO3溶液C.饱和Na2CO3溶液D.水












