某研究小组利用题9图装置探究铜与浓硫酸反应的产物。实验步骤与现象如下:①检查装置气密性 向A中加入5
某研究小组利用题9图装置探究铜与浓硫酸反应的产物。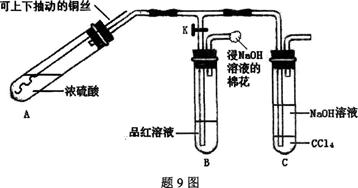 实验步骤与现象如下: ①检查装置气密性,向A中加入5 mL浓硫酸,打开K,将铜丝伸入浓硫酸中,给A处加热,观察到B中品红溶液褪色,再关闭K。 ②实验观察到A中液面下铜丝变黑,产生气泡,液面上方产生大量白雾,一段时间后溶液中有白色固体出现,拉出铜丝,停止加热。回答下列问题: (1)溶液中白色固体是 (填化学式),C中CCl4的作用是 。 (2)取出铜丝,用蒸馏水洗净后伸入到稀硫酸中,铜丝变亮、溶液变蓝。写出A中可能发生反应的化学方程式: 、 。 (3)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生。 ①分离的操作名称为: : ②白色沉淀为: ; ③产生白色沉淀的原因可能是 。 |
参考解答
| (1)CuSO4;防倒吸; (2)Cu+H2SO4(浓)  CuO+SO2↑+H2O;Cu+2H2SO4(浓) CuO+SO2↑+H2O;Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O; CuSO4+SO2↑+2H2O;(3)①分液;② BaSO4;③装置中的O2参与了反应 |
试题分析:(1)浓硫酸在加热时发生反应Cu+2H2SO4(浓)  CuSO4+SO2↑+2H2O。由于在浓硫酸中水很少,所以得到是无水硫酸铜CuSO4,颜色为白色。SO2有漂白性,能使某些有色物质如品红变为无色,因此装置B的品红溶液变为无色。SO2是酸性氧化物,能与NaOH发生反应:SO2+2NaOH=Na2SO3+H2O。导致导气管内的气体压强减小。而引起倒吸现象的发生,但是SO2在CCl4中不容易溶解。因此可以防止倒吸现象的发生。(2)A中可能发生反应的化学方程式为Cu+H2SO4(浓) CuSO4+SO2↑+2H2O。由于在浓硫酸中水很少,所以得到是无水硫酸铜CuSO4,颜色为白色。SO2有漂白性,能使某些有色物质如品红变为无色,因此装置B的品红溶液变为无色。SO2是酸性氧化物,能与NaOH发生反应:SO2+2NaOH=Na2SO3+H2O。导致导气管内的气体压强减小。而引起倒吸现象的发生,但是SO2在CCl4中不容易溶解。因此可以防止倒吸现象的发生。(2)A中可能发生反应的化学方程式为Cu+H2SO4(浓) CuO+SO2↑+H2O;Cu+ 2H2SO4(浓) CuO+SO2↑+H2O;Cu+ 2H2SO4(浓) CuSO4+SO2↑+2H2O;(3)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生。①分离的操作名称为:分液;②Na2SO3+BaCl2=BaSO3↓+2NaCl;2BaSO3 +O2=2BaSO4. BaSO4既不溶于水也不溶于酸。因此白色沉淀为BaSO4。③BaSO3有还原性,O2有氧化性,在溶液中发生氧化还原反应产生白色既不溶于水也不溶于酸沉淀BaSO4。 CuSO4+SO2↑+2H2O;(3)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生。①分离的操作名称为:分液;②Na2SO3+BaCl2=BaSO3↓+2NaCl;2BaSO3 +O2=2BaSO4. BaSO4既不溶于水也不溶于酸。因此白色沉淀为BaSO4。③BaSO3有还原性,O2有氧化性,在溶液中发生氧化还原反应产生白色既不溶于水也不溶于酸沉淀BaSO4。 |
相似问题
分别加入适量下列物质 能使淀粉-KI溶液变蓝的是[ ]A.NaCl B.Fe粉 C.盐酸 D
分别加入适量下列物质,能使淀粉-KI溶液变蓝的是[ ]A.NaCl B.Fe粉 C.盐酸 D.新制氯水
下列有关氯气的叙述中 不正确的是[ ]A.氯气是一种黄绿色 有刺激性气味的气体 B.氯气能溶
下列有关氯气的叙述中,不正确的是[ ]A.氯气是一种黄绿色、有刺激性气味的气体 B.氯气能溶于水C.氯气、液氯和氯水是同一种物质 D.氯气是一种有毒的气体
下列化学实验事实及其结论都正确的是 选项实验事实结论A将SO2通入含HClO的溶液中生成H2SO4H
下列化学实验事实及其结论都正确的是 选项实验事实结论A将SO2通入含HClO的溶液中生成H2SO4HClO的酸性比H2SO4强B铝箔在酒精灯火焰上加热熔化但不滴落铝箔
下图所示的是验证二氧化硫性质的微型实验 a b c d是浸有相关溶液的棉球。将硫酸滴入装有亚硫酸钠固
下图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将硫酸滴入装有亚硫酸钠固体的培养皿中。关于此实验的“现象”、“解释或结
如图 A处通入Cl2 关闭B阀时 C处的红布看不到明显现象;当打开B阀后 C处红布条逐渐褪色。则D瓶
如图,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象;当打开B阀后,C处红布条逐渐褪色。则D瓶中装的是 [ ]A、浓盐酸B、NaOH溶液 C、H2O D、饱和NaCl溶液












