为防治碘缺乏病 通常在食盐中添加少量的碘酸钾(KIO3)。碘酸钾和碘化钾在溶液中能发生下列反应:KI
| 为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3)。碘酸钾和碘化钾在溶液中能发生下列反应:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O (1)该反应中,氧化剂是________,氧化产物是______; (2)当有1 mol I2生成时,有________ mol还原剂被氧化; (3)当有1 mol氧化剂参与反应时,转移电子的数目为________。 |
参考解答
(1)KIO3, I2 (2)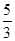 (3)5NA (3)5NA |
试题分析:(1)该反应KIO3+5KI+3H2SO4===3I2+3K2SO4+3H2O中,碘化钾中碘元素的化合价从-1价升高到0价,失去1个电子,被氧化。碘酸钾中碘元素的化合价从+5价降低到0价,得到电子,被还原,因此氧化剂是KIO3,氧化产物是I2。 (2)根据方程式可知,每生成3mol单质碘,反应中转移5mol电子,被氧化的还原剂是5mol,所以当有1 mol I2生成时,有 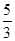 mol还原剂被氧化. mol还原剂被氧化.(3)碘酸钾在反应中得到5个电子,所以当有1 mol氧化剂参与反应时,转移电子的数目为5NA。 |
相似问题
铝可与硝酸钠发生反应(未配平):Al+NaNO+HOAl(OH)+N↑+NaAlO 有关叙述正确的是
铝可与硝酸钠发生反应(未配平):Al+NaNO+HOAl(OH)+N↑+NaAlO,有关叙述正确的是()A.上述反应中水是氧化剂B.若反应过程中转移5 mol e则生成标准
在2KNO3 + S + 3C===K2S + N2↑ + 3CO2↑的反应中 被2molKNO3氧
在2KNO3 + S + 3C===K2S + N2↑ + 3CO2↑的反应中,被2molKNO3氧化的C的质量是A.15gB.18gC.21gD.30g
高锰酸钾和浓盐酸可以发生下列反应:2KMnO4+16HCl(浓)===5Cl2↑+2MnCl2+2K
高锰酸钾和浓盐酸可以发生下列反应:2KMnO4+16HCl(浓)===5Cl2↑+2MnCl2+2KCl+8H2O(1)该反应的氧化剂是______,还原剂是________。(2)若消耗0 2 mol
取一定质量的均匀固体混合物Cu Cu2O和 CuO 将其分成两等份 取其中一份用足量的氢气还原 测得
取一定质量的均匀固体混合物Cu、Cu2O和 CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6 40g,另一份中加入500mL稀硝酸,固
(12分)(1)已知离子反应:+6I—+6H+=R—+3I2+3H2O n= R元素在中的化
(12分)(1)已知离子反应:+6I—+6H+=R—+3I2+3H2O,n=,R元素在中的化合价是。(2)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个












