先阅读下列短文 再回答下列问题:在酸性条件下 次氯酸钠(NaClO) 过氧化氢都有很强的氧化性 可将
先阅读下列短文,再回答下列问题: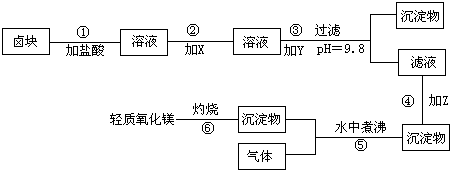 在酸性条件下,次氯酸钠(NaClO)、过氧化氢都有很强的氧化性,可将Fe2+氧化为Fe3+.Mg(OH)2和Fe(0H)3在溶液中生成时呈胶状物或絮状物沉淀,而MgCO3在水中煮沸可转变为Mg(OH)2.“卤块”的主要成分为MgCl2,还含有FeCl2、FeCl3、MnCl2等杂质.若以它为原料,按如图工艺流程即可制得“轻质氧化镁”.若要求产品不含杂质离子,而且成本较低,流程中所用试剂或pH控制可参考表1、表2来确定. 表1:
(1)写出盐酸溶液中NaClO将FeCl2氧化成FeCl3,同时生成NaCl和H2O的化学方程式:______,写出在盐酸溶液中H2O2将FeCl2氧化成FeCl3,同时生成H2O的化学方程式:______. (2)在步骤2中加入物质X,最佳的选择应是______,理由是______. (3)在步骤3中加入的物质应是______,之所以要控制pH=9.8,其目的是______. (4)在步骤4中加入物质应是______. (5)在步骤5中发生的化学方程式为______. |
参考解答
| (1)NaClO将FeCl2氧化成FeCl3,同时生成NaCl和水,H2O2将FeCl2氧化成FeCl3,并生成了水,所以本题答案为:NaClO+2FeCl2+2HCl═2FeCl3+NaCl+H2O,H2O2+2HCl+2FeCl2═2FeCl3+2H2O; (2)要加入的X为过氧化氢或次氯酸钠,根据反应的原理可以看出,次氯酸钠作为氧化剂反应后生成氯化钠杂质,而过氧化氢生产的是水,且次氯酸钠的价格高于过氧化氢,所以加入过氧化氢合适,所以本题答案为:过氧化氢,使用H2O2溶液成本低,且不含其他杂质离子; (3)要得到较为纯净的氧化镁,需将卤块中含有的杂质除掉,根据表格提供的信息可以看出,氢氧化镁在pH、为9.6时开始形成沉淀,故要控制pH=9.8,所以本题答案为:氢氧化钠,不使氯化镁形成沉淀; (4)MgCO3在水中煮沸可转化为更难溶的Mg(OH)2,所以加入的Z可以是碳酸钠,所以本题答案为:碳酸钠; (5)碳酸镁能与水在加热时生成氢氧化镁和二氧化碳,所以本题答案为:MgCO3+H2O
故答案为:(1)NaClO+2FeCl2+2HCl═NaCl+2FeCl3+H2O;H2O2+2FeCl2+2HCl═2FeCl3+2H2O (2)过氧化氢溶液;使用H2O2溶液成本低,且不含其他杂质离子 (3)NaOH溶液;使FeCl3、MnCl2都转化为Fe(OH)3、Mn(OH)2沉淀,而大部分MgCl2尚未转化为Mg(OH)2,仍以MgCl2留在滤液中,达到分离杂质的目的 (4)碳酸钠; (5)MgCO3+H2O
|
相似问题
在一定条件下 下列转化不能由一步反应实现的是( )A.CO2→CaCO3B.HCl→NaClC.F
在一定条件下,下列转化不能由一步反应实现的是( )A.CO2→CaCO3B.HCl→NaClC.Fe2O3→FeSO4D.Ca(OH)2→NaOH
用铝屑 稀硫酸 氢氧化钠溶液制备Al(OH)3有如下三种方案:方案一:2Al+3H2SO4=Al2(
用铝屑,稀硫酸,氢氧化钠溶液制备Al(OH)3有如下三种方案:方案一:2Al+3H2SO4=Al2(SO)3+3H2↑Al2(SO)3+6NaOH=2Al(OH)3↓+3Na2SO4方案二:2Al+2N
根据下图所示的转化关系 推断甲物质是( )甲盐酸乙硝酸银溶液丙铁丁氧气甲.A.CuB.CuOC.M
根据下图所示的转化关系,推断甲物质是( )甲盐酸乙硝酸银溶液丙铁丁氧气甲.A.CuB.CuOC.MgOD.Mg
某化合物X可分别由CuO Cu(OH)2 CuSO4和CuCO3 通过化学反应制得 则X的化学式可能
某化合物X可分别由CuO、Cu(OH)2、CuSO4和CuCO3,通过化学反应制得,则X的化学式可能是______或______.
A是植物发酵得到的一种有机染料 请根据下列转化关系回答:(1)若该有机染料的化学式为CH3OH或C2
A是植物发酵得到的一种有机染料,请根据下列转化关系回答:(1)若该有机染料的化学式为CH3OH或C2H5OH.为了确定该有机物的成分,去一定量该无色液体A在












