200 ℃时 11.6 g CO2和水蒸气的混合气体与足量的Na2O2充分反应后 固体质量增加了3.
| 200 ℃时,11.6 g CO2和水蒸气的混合气体与足量的Na2O2充分反应后,固体质量增加了3.6 g。求混合物中CO2和H2O的质量比。 |
参考解答
| 设混合物中CO2和H2O的质量分别为x、y。 2CO2+2Na2O2====2Na2CO3+O2Δm 88 56 x 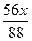 2H2O+2Na2O2====4NaOH+O2↑ Δm 36 4 y 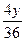 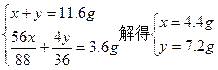 故:m(CO2)∶m(H2O)=4.4∶7.2=11∶18。 混合物中CO2和H2O的质量比为11∶18。 |
| 本题可用“差量法”解题,设未知数,列方程组求解。 |
相似问题
在1.00 L 1.00 mol·L-1 NaOH溶液中通入16.8 L标准状况下的CO2 计算所得
在1 00 L 1 00 mol·L-1 NaOH溶液中通入16 8 L标准状况下的CO2,计算所得溶液中含有的NaHCO3和Na2CO3的物质的量分别为________。
下列各物质中的杂质(括号内)可用加热的方法除去的是( )①Na2O2(Na2O) ②NaHCO3
下列各物质中的杂质(括号内)可用加热的方法除去的是()①Na2O2(Na2O)②NaHCO3(Na2CO3)③Na2CO3(NaHCO3)④NaOH(NaHCO3)A.①②B.①③C.①④D.③④
取a g某物质A 在氧气中完全燃烧 使燃烧产物跟足量过氧化钠反应 反应后固体的质量增加了b g。若b
取a g某物质A,在氧气中完全燃烧,使燃烧产物跟足量过氧化钠反应,反应后固体的质量增加了b g。若b>a,则A为( )A.H2B.COC.C12H22O11D.C6H12O6
下列关于Na2O和Na2O2的叙述正确的是 [ ]A.都是白色固体 B.都是碱性氧化物 C.
下列关于Na2O和Na2O2的叙述正确的是 [ ]A 都是白色固体 B 都是碱性氧化物 C 都能和水反应形成强碱溶液 D 都是强氧化剂
下列物质与氧气反应 生成氧化物的种类最少的是 ( )A.LiB.NaC.KD.Rb
下列物质与氧气反应,生成氧化物的种类最少的是()A.LiB.NaC.KD.Rb












