在饱和Na2CO3溶液中通入二氧化碳会有晶体析出 在饱和NaCl溶液中通入CO2则不发生化学反应。若
| 在饱和Na2CO3溶液中通入二氧化碳会有晶体析出,在饱和NaCl溶液中通入CO2则不发生化学反应。若在饱和NaCl溶液中通入氨气后,再通入CO2则会有晶体析出,简述其原因并写出相应的化学方程式。 |
参考解答
| 饱和Na2CO3溶液中通入CO2时,所发生的化学反应是:Na2CO3+CO2+H2O==== 2NaHCO3;在饱和NaCl溶液中通入足量氨气以后再通入CO2时,则发生以下反应: NH3+CO2+H2O====NH4HCO3 NH4HCO3+NaCl====NH4Cl+NaHCO3↓ 其中NaHCO3溶解度最小,故有NaHCO3的晶体析出。 |
| 在Na2CO3饱和溶液中通入CO2时,由于Na2CO3易溶于水,且发生反应Na2CO3+CO2+H2O ====2NaHCO3,而生成的NaHCO3溶解度小,所以随着CO2气体的通入,会有NaHCO3晶体析出。 氯化钠是强酸盐,CO2是弱酸的酸酐,根据复分解反应规律,CO2不能与NaCl溶液反应。通入足量氨气的饱和NaCl溶液中再通入CO2时,CO2跟氨水反应生成NH4HCO3,当溶液中Na+、Cl-、 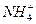 、 、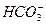 等离子浓度都较大时,首先是微溶于水的NaHCO3析出。 等离子浓度都较大时,首先是微溶于水的NaHCO3析出。 |
相似问题
下列“反应”中不是化学反应的是 ( )A.显色反应B.焰色反应C.颜色反应D.水解反应
下列“反应”中不是化学反应的是 ( )A.显色反应B.焰色反应C.颜色反应D.水解反应
做钠与水的反应实验时 不能用很大的钠块 原因是( )A.大的钠块会沉于水底B.钠不易反应完C.容易发
做钠与水的反应实验时,不能用很大的钠块,原因是()A.大的钠块会沉于水底B.钠不易反应完C.容易发生爆炸而迸溅D.会使水沸腾
有Na2SO4和Na2CO3混合溶液10.0mL 加入足量BaCl2溶液 充分反应后 经过滤 洗涤
有Na2SO4和Na2CO3混合溶液10 0mL,加入足量BaCl2溶液,充分反应后,经过滤、洗涤、烘干,得到白色沉淀1 45g,将沉淀与过量的盐酸反应,得到112mLCO2气体
(18分)(1)标准状况下 44.8L的NH3气体质量为 g 其中含
(18分)(1)标准状况下,44 8L的NH3气体质量为g,其中含 个氮原子,其中含 mol 氢原子。(2)标准状况下,11 2L的H2R气体质量为17g,则H2R的摩尔质
一块表面已部分被氧化的钠的质量为0.77 g 放入10 g水中后 得到氢气0.02 g。求:(1)金
一块表面已部分被氧化的钠的质量为0 77 g,放入10 g水中后,得到氢气0 02 g。求:(1)金属钠表面氧化钠的质量;(2)所得溶液的质量分数;(3)被氧化前这块钠的质量。












