将表面已被部分氧化为Na2O的5.40 g金属钠放入40.0 mL(4 ℃)水中 在标准状况下收集到
| 将表面已被部分氧化为Na2O的5.40 g金属钠放入40.0 mL(4 ℃)水中,在标准状况下收集到1.12 L氢气(ρ="0.089" 9 g·L-1)。试求: (1)原混合物中钠和氧化钠的质量。 (2)所得NaOH溶液中溶质的质量分数。 |
参考解答
| (1)m(Na)='2.32' g,m(Na2O)='3.08' g; (2)17.7%(或0.177) |
| (1)m(H2)='1.12' L×0.089 9 g·L-1='0.101' g 2Na+2H2O='===2NaOH ' + H2↑ 46 80 2 m(Na) m1(NaOH) 0.101 g m(Na)='2.32' g。 m(Na2O)='5.40' g-2.32 g='3.08' g。 (2)m1(NaOH)='4.04' g Na2O+H2O====2NaOH 62 80 3.08 g m2(NaOH) m2(NaOH)='3.97' g m总(NaOH)='4.04' g+3.97 g='8.01' g m(NaOH溶液)='40.0' g+5.40 g-0.101 g ='45.3' g w (NaOH)= 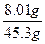 ×100%=17.7%。 ×100%=17.7%。 |
相似问题
18.6g NaOH和Na2CO3的固体混合物投入200ml 2.0mol·L-1的盐酸中恰好完全反
18 6g NaOH和Na2CO3的固体混合物投入200ml 2 0mol·L-1的盐酸中恰好完全反应,不再产生气泡,则所得溶液中溶质的质量为多少A.25 8gB.11 7gC.23 4gD.无法计算
将一块部分被氧化的金属钠(假设氧化产物只有Na2O2)投入盛满水且倒置水槽内的容器中 此时在容器中可
将一块部分被氧化的金属钠(假设氧化产物只有Na2O2)投入盛满水且倒置水槽内的容器中,此时在容器中可收集到448mL(标准状况)气体(假定各步反应完全,并产生
有50mL NaOH溶液 向其中逐渐通入一定量的CO2 随后向溶液中逐滴加入0.1mol/L的盐酸
有50mL NaOH溶液,向其中逐渐通入一定量的CO2,随后向溶液中逐滴加入0 1mol L的盐酸,产生的CO2气体体积(标准状况)与所加入的盐酸的体积之间的关系如
下列有关钠的叙述中 不正确的是A.钠的还原性很强 可以用来冶炼金属钛 锆 铌等B.钠的化学性质非常活
下列有关钠的叙述中,不正确的是A.钠的还原性很强,可以用来冶炼金属钛、锆、铌等B.钠的化学性质非常活泼,钠元素只能以化合态存在于自然界C.钠燃烧发
下列实验不能验证Na2O2与H2O反应后的溶液中存在大量H2O2的是A.向溶液中加入酚酞试剂B.向溶
下列实验不能验证Na2O2与H2O反应后的溶液中存在大量H2O2的是A.向溶液中加入酚酞试剂B.向溶液中加入MnO2粉末C.向溶液中通入CO2气体D.向溶液中加入KMnO4溶液












