(14分)(1) 把除去氧化膜的铁丝投入到盛有稀硫酸的试管中 产生氢气 的速率变化情况如图所示图中t
(14分)(1) 把除去氧化膜的铁丝投入到盛有稀硫酸的试管中,产生氢气 的速率变化情况如图所示图中t1~t2速率变化的主要原因是 ,t2~t3速率变化的主要原因是 。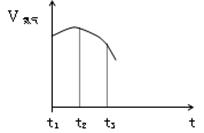 (2)甲、乙、丙、丁是四种短周期元素,乙原子中K层与M层电子数相等;甲原子的核 外电子数比乙原子核外电子数少1;丙原子的最外层电子数是次外层电子数的2倍;丁原子核电荷数比丙原子核电荷数多2。请回答: ①甲的单质与水反应的离子方程式为 ;②乙元素在周期表中的位置为 ;③丙元素的最高价氧化物的电子式为 ;④甲与丁两种元素可组成的具有强氧化性的物质是 。(填化学式) (3)某元素R,它的最高价含氧酸的阴离子是RO4ˉ,则其气态氢化物的化学式是 。 |
参考解答
| (1) 铁与硫酸的反应是放热反应,溶液温度升高,反应速率加快;(放热反应1分;温度升高1分) 硫酸酸浓度减小,反应速率减慢。(浓度减小给2分) (2)2Na+2H2O==2Na++2OH-+H2↑ ;第三周期第ⅡA族 ; 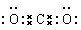 ;Na2O2 ;Na2O2 (3)HR |
试题分析:(1)把除去氧化膜的铁丝投入到盛有稀硫酸的试管中,产生氢气的速率变化情况如右图所示图中t1~t2速率变化的主要原因是铁与硫酸的反应是放热反应,放出热量是溶液的温度升高,升高温度,化学反应速率加快;随着反应的进行,溶液变稀,这时影响化学反应速率的主要因素是物质的浓度。由于t2~t3时主要是物质浓度的影响,所以化学反应速率减慢。(2)根据题意可知甲是Na;乙是Mg;丙是C;丁是O。①甲的单质与水反应的离子方程式为2Na+2H2O==2Na++2OH-+H2↑;②乙元素在周期表中的位置为第三周期第ⅡA族;③丙元素的最高价氧化物的电子式为 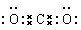 ;④甲与丁两种元素可组成的具有强氧化性的物质的化学式是Na2O2。(3)某元素R,它的最高价含氧酸的阴离子是RO4ˉ,则其最高化合价是+7价,由于同一种元素的最高化合价与最低化合价绝对值的和为8,在其氢化物中为最低化合价,所以为-1价,则其气态氢化物的化学式是HR。 ;④甲与丁两种元素可组成的具有强氧化性的物质的化学式是Na2O2。(3)某元素R,它的最高价含氧酸的阴离子是RO4ˉ,则其最高化合价是+7价,由于同一种元素的最高化合价与最低化合价绝对值的和为8,在其氢化物中为最低化合价,所以为-1价,则其气态氢化物的化学式是HR。 |
相似问题
经分析 某物质中只有一种元素 则此物质[ ]A.一定是一种单质 B.一定是纯净物 C.一定是
经分析,某物质中只有一种元素,则此物质[ ]A.一定是一种单质 B.一定是纯净物 C.一定是混合物 D.可能是纯净物也可能是混合物
目前 医疗上使用放射性核素治疗肿瘤 该核素原子核内的中子数与电子数之差是A.125B.72C.19D
目前,医疗上使用放射性核素治疗肿瘤,该核素原子核内的中子数与电子数之差是A.125B.72C.19D.53
下列有关物质分类或归类正确的一组是[ ]①液氨 液氯 干冰 碘化银均为化合物 ②氢氟酸 盐酸
下列有关物质分类或归类正确的一组是[ ]①液氨、液氯、干冰、碘化银均为化合物 ②氢氟酸、盐酸、水玻璃、氨水均为混合物③明矾、小苏打、醋酸、次氯酸
将下列各组物质按酸 碱 盐分类顺序排列 正确的是[ ]A.硫酸 纯碱 石灰石 B.醋酸 烧碱
将下列各组物质按酸、碱、盐分类顺序排列,正确的是[ ]A.硫酸,纯碱,石灰石 B.醋酸,烧碱,氯化亚铁C.磷酸,苛性钠,水玻璃D.次氯酸,火碱,漂白粉
如图所示是元素周期表的一部分 X Y Z W均为短周期元素 若W原子最外层电子数是其内层电子数的7/
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若W原子最外层电子数是其内层电子数的7 10。则下列说法中不正确的是A.原子半径由大到小排列












