提示:在本实脸条件下 Ni(Ⅱ)不能被氧化:高锰酸钾的还原产物是MnO2回答下列问题:(1)反应②中
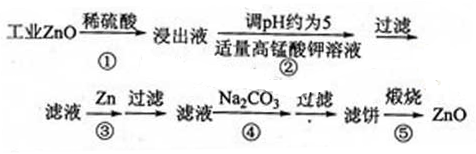 提示:在本实脸条件下,Ni(Ⅱ)不能被氧化:高锰酸钾的还原产物是MnO2 回答下列问题: (1)反应②中除掉的杂质离子是 ,发生反应的离子方程式为 ;在加高锰酸钾溶液前,若pH较低,对除杂的影响是 。 (2)反应③的反应类型为 ,过滤得到的滤渣中,除了过量的锌外还有 。 (3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是 。 (4)反应④中产物的成分可能是ZnCO3·xZn(OH)2取干操后的滤饼11.2g,煅烧后可得到产品8.1g,则x等于 。 |
参考解答
| (1)Fe2+和Mn2+; MnO4-+3Fe2++7H2O=MnO2↓+3Fe(OH)3↓+5H+; 3Mn2++2MnO4-+2H2O===5MnO2↓+4H+;不会形成Fe(OH)3和MnO2沉淀。或无法除去Fe2+和Mn2+; (2)置换反应;Ni (3)取最后一次洗涤液少量,滴入稀盐酸,加入氯化钡溶液,没有白色沉淀生成,证明洗涤干净。 (4)1 |
(1)根据题意,Ni(Ⅱ)不能被氧化,反应②中除掉的杂质离子是Fe2+和Mn2+,发生的离子方程式为MnO4-+3Fe2++7H2O=3Fe(OH)3↓+MnO2↓+5H+、2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;加高锰酸钾溶液前,若pH较低,铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质; (2)反应③为锌与镍离子的发生反应得到锌离子和镍,反应类型为置换反应;得到的滤渣中,除了过量的锌外还有金属镍。 (3)取最后一次少量水洗夜于试管中,滴入1~2滴稀硝酸,再滴入硝酸钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净。 (4)根据关系式 ZnCO3?xZn(OH)2~(x+1)ZnO 125+99x 81(x+1) 11.2g 8.1g 解得:x=1 |
相似问题
含有a mol FeBr2的溶液中 通入x mol Cl2。下列各项为通Cl2过程中 溶液内发生反应
含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是A.x=0 4a,2Fe2++Cl2=2Fe3++2C
下列过程的离子方程式正确的是A.用烧碱溶液吸收Cl2:Cl2+2OH- =Cl-+ClO-+H2OB
下列过程的离子方程式正确的是A.用烧碱溶液吸收Cl2:Cl2+2OH- =Cl-+ClO-+H2OB.用饱和Na2CO3溶液转化锅垢中的CaSO4:CaSO4(s)+CO32- (aq)=CaCO3(s)+SO
Co在化合物中呈现的价态类似于铁。已知Co(OH)2在空气中加热时 固体残留率随温度的变化如图所示。
Co在化合物中呈现的价态类似于铁。已知Co(OH)2在空气中加热时,固体残留率随温度的变化如图所示。已知钴的氢氧化物加热至290℃时已完全脱水。下列说法正
在离子浓度都为0.1 mol·L-l的下列溶液中 加入(通入)某物质后 发生反应的先后顺序排列正确的
在离子浓度都为0.1 mol·L-l的下列溶液中,加入(通入)某物质后,发生反应的先后顺序排列正确的是A.在含Ag+、Cu2+的溶液中加入Zn:Ag+、Cu2+B.在含Fe3
下列反应中 属于氧化还原反应的是[ ]A.2H2O22H2O + O2↑B.2Al(OH)3
下列反应中,属于氧化还原反应的是[ ]A.2H2O22H2O + O2↑B.2Al(OH)3Al2O3 + 3H2O C.FeO + 2HCl = FeCl2 + H2O D.CuCl2 + 2NaOH = Cu(OH)2↓+ 2NaCl












