A B C和D等4种元素 A元素所处的周期数 主族序数 原子序数均相等;B的原子半径是其所在主族中最
| A、B、C和D等4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C. (1)B在周期表中的位置第______周期,第______族; (2)A、B形成的化合物的电子式______; (3)C的元素名称______,C的最高价氧化物的化学式______; (4)D的最高价氧化物对应的水化物的化学式______. |
参考解答
| A元素所处的周期数、主族序数、原子序数均相等,则A为H元素;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3,则B在第二周期第ⅤA族,即B为N元素;C元素原子的最外层电子数比次外层少2个,则C有3个电子层,最外层电子数为6,即C为S元素;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C,则D为第四周期第ⅠA族元素,即D为K元素, (1)B为N元素,位于元素周期表中第二周期第ⅤA族,故答案为:二;第ⅤA族; (2)A、B形成的化合物为NH3,其电子式为 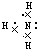 ,故答案为: 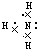 ; (3)C为S元素,其名称为硫,最外层电子数为6,则最高正价为+6,所以最高价氧化物的化学式SO3,故答案为:硫;SO3; (4)D为K,其最高价氧化物对应的水化物的化学式为KOH,故答案为:KOH. |
相似问题
下图为元素周期表的一部分 已知A B C D E5种元素的原子核外共有85个电子 E原子核外有4个
下图为元素周期表的一部分,已知A, B,C,D,E5种元素的原子核外共有85个电子,E原子核外有4个电子层,则B元素是[ ]A.Si B.P C.S D.Cl
X Y为短周期元素 X原子各电子层的电子数比为1:4:1 它比Y原子多3个电子.下列叙述正确的是(
X、Y为短周期元素,X原子各电子层的电子数比为1:4:1,它比Y原子多3个电子.下列叙述正确的是( )A.X离子半径大于Y离子半径B.X单质在空气中燃烧可
下列叙述中 正确的是[ ]A.两种微粒 若核外电子排布完全相同 则其化学性质一定相同B.凡单
下列叙述中,正确的是[ ]A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布C
以下对核外电子运动状况的描述正确的是 [ ]A.电子的运动与行星相似 围绕原子核在固定的轨道
以下对核外电子运动状况的描述正确的是 [ ]A.电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转 B.能量低的电子只能在s轨道上运动,能量高的
已知A B C D E是五种短周期元素 它们的原子序数依次增大.A元素原子形成的离子只有一个质子;C
已知A、B、C、D、E是五种短周期元素,它们的原子序数依次增大.A元素原子形成的离子只有一个质子;C、D、E三种元素的最高价氧化物对应水化物之间两两可以












