现有A B C D E五种核电荷数小于18的元素 其中:A原子核内无中子 B原子最外层电子数是次外层
| 现有A、B、C、D、E五种核电荷数小于18的元素,其中:A原子核内无中子,B原子最外层电子数是次外层的2倍,C原子最外层电子数是其电子层数的3倍,D原子核外K层比M层电子数多1,,E形成的-1价离子与Ar原子核外电子排布相同; 由此推知: (1)A原子符号是______; (2)B原子结构示意图是______ (3)E元素形成的单质与A、C、D三元素形成呈碱性的化合物反应的方程式: ______. |
参考解答
| 由题意可知:A为H元素,B为C元素,C为O元素,D为Na元素,E为Cl元素, (1)因A为H元素,则A原子符号是11H,故答案为:11H; (2)B为C元素,C原子结构示意图为: 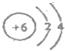 ,故答案为: 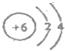 ; (3)E的单质为Cl2,A、C、D三元素形成呈碱性的化合物为NaOH,两者反应的方程式:2NaOH+Cl2═NaCl+NaClO+H2O,故答案为:2NaOH+Cl2═NaCl+NaClO+H2O. |
相似问题
已知aAn+ bB(n+1)+ cCn- dD(n+1)- 均具有相同的电子层结构 下列判断正确的是
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均具有相同的电子层结构,下列判断正确的是( )A.元素的金属性:B>A>C>DB.原子半径:A>B>D>CC.离子
短周期元素A B C D原子序数依次增大 且只有C为金属元素.A C位于同一主族 B的最外层电子数是
短周期元素A、B、C、D原子序数依次增大,且只有C为金属元素.A、C位于同一主族,B的最外层电子数是次外层的3倍,B、C的最外层电子数之和与D的最外层电子
A元素最高正价和负价绝对值之差为6 B元素次外层有8个电子 BA2在水溶液中能电离出相同电子层结构的
A元素最高正价和负价绝对值之差为6,B元素次外层有8个电子,BA2在水溶液中能电离出相同电子层结构的离子,则BA2是( )A.MgCl2B.CaCl2C.NO2D.CO2
已知aAn+ bB(n+1)+ cCn- dD(n+1)-具有相同的电子层结构 关于A B C D四
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是( )A.这四种离子的电子层结构相同,因而离子
X Y Z三种元素原子序数之和为36 X Y在同一周期 X+和Z2-具有相同电子层结构 下列推断错误
X、Y、Z三种元素原子序数之和为36,X、Y在同一周期,X+和Z2-具有相同电子层结构,下列推断错误的是( )A.X是同周期元素中金属性最强的元素B.原子半












