X Y Z W为原子序数依次增大的四种短周期主族元素 其中X Z同族 W Z同周期 Y是短周期主族元
| X、Y、Z、W为原子序数依次增大的四种短周期主族元素,其中X、Z同族,W、Z同周期,Y是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,W的最高正价与最低负价代数和为6. (1)X元素的名称是______.该元素在周期表中的位置为______. (2)Y元素符号是______Y元素的原子结构示意图为______. (3)X、Y、Z三种元素按原子半径由大到小的顺序排列为______(用元素符号填空). (4)X、Y、Z、W四种元素的最高价氧化物对应的水化物酸性最强的是______碱性最强的是______ (用化学式填空) (5)写出 Y元素的最高价氧化物对应的水化物和W元素的最高价氧化物对应的水化物反应的离子方程式______. |
参考解答
| X、Y、Z、W为原子序数依次增大的四种短周期主族元素,Y是短周期主族元素中原子半径最大的,则Y为Na,X原子最外层电子数是核外电子层数的3倍,X为第二周期元素,则质子数为8,即X为O;X、Z同族,Z为S;W、Z同周期,W的最高正价与最低负价代数和为6,则W为第三周期第ⅤⅡA族元素,即W为Cl, (1)X为O,其名称为氧,原子结构中有2个电子层,最外层电子数为6,则在元素周期表中第二周期第ⅥA族,故答案为:氧;第二周期第ⅥA族; (2)Y为Na,其质子数为11,有3个电子层,最外层电子数为1,则原子结构示意图为 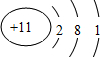 ,故答案为:Na; 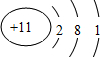 ; (3)Na、S在同周期,原子半径在减小,O的电子层数最少,则半径最小,则原子半径为Na>S>O, 故答案为:Na>S>O; (4)上述几种元素中Cl的非金属性最强,则HClO4的酸性最强,Na的金属性最强,则NaOH的碱性最强, 故答案为:HClO4;NaOH; (5)Y元素的最高价氧化物对应的水化物为NaOH,W元素的最高价氧化物对应的水化物为HClO4,分别为强碱、强酸,离子反应为OH-+H+=H2O,故答案为:OH-+H+=H2O. |
相似问题
基态氮原子的电子排布为1s22s22p3 则氮原子的p轨道上三个电子的排布式为 [ ]A.
基态氮原子的电子排布为1s22s22p3,则氮原子的p轨道上三个电子的排布式为 [ ]A. B. C. D.
短周期A B C D 四种元素 原子序数依次增大 A原子的最外层上有4个电子;B的阴离子和C的阳离子
短周期A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,可生成一种原
下列说法正确的是( )A.阴阳离子间通过静电吸引形成的化学键叫做离子键B.HF HCl HBr H
下列说法正确的是( )A.阴阳离子间通过静电吸引形成的化学键叫做离子键B.HF,HCl,HBr,HI的热稳定性和酸性均依次减弱C.同种非金属元素的化合价越
有aXn-和bYm+两种单原子离子 它们的电子层结构相同 下列关系式或化学式正确是( )A.a-n
有aXn-和bYm+两种单原子离子,它们的电子层结构相同,下列关系式或化学式正确是( )A.a-n=b+mB.X的氢化物化学式为HnX或XHnC.a+n=b+mD.Y的氧化物化学式为YOm
X Y Z W R是5种短周期元素 其原子序数依次增大.X是周期表中原子半径最小的元素 Y原子最外层
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与












