下图是用铅蓄电池为电源 模拟氯碱工业电解饱和食盐水的装置图(C D均为石墨电极)。已知:铅蓄电池在放
下图是用铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。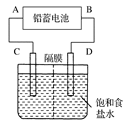 已知:铅蓄电池在放电时发生下列电极反应 负极 Pb+ 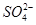 -2e-===PbSO4 -2e-===PbSO4正极 PbO2+4H++ 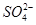 +2e-===PbSO4+2H2O +2e-===PbSO4+2H2O(1)请写出电解饱和食盐水的化学方程式 。 (2)若在电解池中C极一侧滴2滴酚酞试液,电解一段时间后未呈红色,说明蓄电池的A极为________极。 (3)用铅蓄电池电解1 L饱和食盐水(食盐水足量、密度为1.15 g·cm-3)时, ①若收集到11.2 L(标准状况下)氯气,则至少转移电子________mol。 ②若蓄电池消耗H2SO4 2 mol,则可收集到H2的体积(标准状况下)为________L。 |
参考解答
(8分)(1)2NaCl+2H2O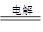 2NaOH+Cl2↑+H2↑ (2)正 (3)①1 ②22.4 2NaOH+Cl2↑+H2↑ (2)正 (3)①1 ②22.4 |
试题分析:(1)惰性电极电解饱和食盐水的化学方程式为2NaCl+2H2O  2NaOH+Cl2↑+H2↑。 2NaOH+Cl2↑+H2↑。(2)若在电解池中C极一侧滴2滴酚酞试液,电解一段时间后未呈红色,这说明C电极应该是电解池的阳极,溶液中的氯离子放电,所以蓄电池的A极为正极。 (3)①氯气的物质的量是11.2L÷22.4L/mol=0.5mol,则根据电极反应式2Cl--2e-=Cl2↑可知,反应中转移电子的物质的量是0.5mol×2=1.0mol。 ②根据蓄电池的电极反应式可知,消耗2mol硫酸,反应中就转移2mol电子。所以若蓄电池消耗H2SO4 2 mol,则反应中转移2mol电子,因此根据电极反应式2H++2e-=H2↑可知,可收集到H2的物质的量是1mol,其体积(标准状况下)为22.4L。 点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固与训练,有利于培养学生灵活运用基础知识解决实际问题的能力,有助于提高学生的应试能力和学习效率。 |
相似问题
根据图示判断下列叙述符合事实的是A.按图①连接并放置一段时间后 Fe片表面会“镀”上一层铜B.按图②
根据图示判断下列叙述符合事实的是A.按图①连接并放置一段时间后,Fe片表面会“镀”上一层铜B.按图②连接好导线后(Zn片与Cu片相接触),灵敏电流表会发
用酸性氢氧燃料电池为电源进行电解的实验装置如下图所示。下列说法正确的是( ) A.a为负极 b
用酸性氢氧燃料电池为电源进行电解的实验装置如下图所示。下列说法正确的是( ) A.a为负极,b为正极B.若a极是铁,b极是铜,b极逐渐溶解,a极上有铜析
钢铁腐蚀发生得最普遍的是 ( )A.吸氧腐蚀B.析氢腐蚀C.化学腐蚀D.摩擦损耗
钢铁腐蚀发生得最普遍的是()A.吸氧腐蚀B.析氢腐蚀C.化学腐蚀D.摩擦损耗
全世界短年钢铁因锈蚀造成大量的损失。某城市拟用如图方法保护埋在酸性土壤中的钢质管道 使其免受腐蚀。关
全世界短年钢铁因锈蚀造成大量的损失。某城市拟用如图方法保护埋在酸性土壤中的钢质管道,使其免受腐蚀。关于此方法,下列说法不正确的是A.土壤中的钢铁
据环保部门测定 我国一些大城市的酸雨pH=3.5。在酸雨季节铁制品极易腐蚀 则在其腐蚀中正极发生的反
据环保部门测定,我国一些大城市的酸雨pH=3 5。在酸雨季节铁制品极易腐蚀,则在其腐蚀中正极发生的反应是 ( )。A.Fe-2e-=Fe2+B.2H2O+O2+4e-












