过氧化钠(化学式为Na202)可用在呼吸面具中作为氧气来源。Na202能跟C02反应生成02和另一种
| 过氧化钠(化学式为Na202)可用在呼吸面具中作为氧气来源。Na202能跟C02 反应生成02和另一种固体化合物(用X表示);它也能跟H20反应生成02,化学方程式 为:2Na202+2H20=4NaOH+02↑。以下是某兴趣小组进行的探究活动。 (1)利用如下图所示实验装置制取氧气,请回答有关问题。 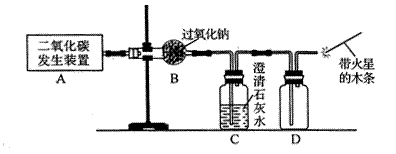 ①实验室制取CO2的化学方程式为 。 ②表明C02未被Na202完全吸收的实验现象为 。 ③O2可采用D装置收集,并用带火星的木条检验,这是利用了O2的哪些性质? ④若A装置产生的C02中混有水蒸气,要检验干燥的C02能否与Na202反应生成 O2,以上实验装置应如何改进? (2)为探究X是哪种物质及其有关性质,同学们进行了如下分析和实验。 ①有同学猜想X可能是酸、碱或盐中的一种。通过对物质组成的分析,大家一致认为X肯定不是酸和碱,理由是 。 ②同学们通过讨论和实验证明了X是Na2C03。以下是他们设计的有关Na2C03性质的探究实验,请根据卷首资料提供的信息,将下表填写完整。
(3)7.8g过氧化钠与足量的水反应,生成氧气的质量是多少?若反应后得到了40g 氢氧化钠溶液,请计算氢氧化钠溶液中溶质的质量分数。 |
参考解答
| (1)CaC03+2HCl==CaCl2+H20+C02↑ ②澄清石灰水变浑浊 ③氧气密度比空气的大,氧气有助燃性。 ④在A、B装置之间和B、C装置之间增加气体干燥装置(答出在A、B装置之间增加 气体干燥装置即可)。  (2)①Na202和C02都不含氢元素,根据质量守恒定律,二者反应后不可能生成含氢 (2)①Na202和C02都不含氢元素,根据质量守恒定律,二者反应后不可能生成含氢元素的酸或碱 ② ’
(3)解:设生成氧气的质量为x,生成氢氧化钠的质量为y。 2Na202+2H20=4NaOH+02↑ 156 160 32  7.8g y x X=1.6g Y=8g 氢氧化钠溶液中溶质的质量分数为: 8g/40g×100%=20% 答:略。 |
| (1)①实验用大理石或石灰石与稀盐酸反应制取CO2气体,其反应的化学方程式为CaCO3+2HC1=CaC12+H2O+CO2↑;②装置C是检验CO2是否被完全吸收的,若澄清石灰水变浑浊,表明CO2未被完全吸收;③在收集装置中“长进短出”说明了O2的密度大于空气密度,且氧气能助燃;④A中产生的CO2中带有水蒸气,要除去需在A和B间增加气体干燥装置,要保证是干燥CO2与Na2O2反应还需在B、C之间增加干燥装置,以防C装置中水蒸气进入B干扰实验。(1)①由质量守恒定律知:反应前后原子的种类不会改变,即Na2O2和CO2反应不可能生成酸和碱中的氢元素;②Na2CO3的检验要加入稀HC1观察是否有气泡产生,为了排除产生所体的氢气,常将产生的气体通入澄清石灰水中观察其是否变为浑浊,从而确定碳酸盐的存在,也可加入含Ca2+或Ba2+的溶液(如CaC12、BaC12等)看是否有沉淀生成。③生成氧气的质量可由参加反应的7.8g Na2O2利用化学方程式求得,同时生成NaOH的质量也可由7.8g Na2O2的质量求得,然后利用溶质质量分数的计算公式,求得NaOH溶液中溶质的质量分数 |
相似问题
(2008·宜昌)实验室常用下列装置研究气体的制取和性质 根据所学知识回答下列问题。(1)写出实验室
(2008·宜昌)实验室常用下列装置研究气体的制取和性质,根据所学知识回答下列问题。(1)写出实验室制取氧气的一个化学方程式____________。利用该反应制取
( 11分)实验室制取氧气的实践与研究。⑴过氧化氢是一种无色透明的无毒液体 过氧化氢溶液俗称“双氧水
( 11分)实验室制取氧气的实践与研究。⑴过氧化氢是一种无色透明的无毒液体,过氧化氢溶液俗称“双氧水”,具有强氧化性。贮运过氧化氢的试剂箱上最适
在进行物质分类时 一般将纯净物分为单质(包括金属单质 非金属单质和稀有气体单质)和化合物。我们已经学
在进行物质分类时,一般将纯净物分为单质(包括金属单质、非金属单质和稀有气体单质)和化合物。我们已经学习了氧气的化学性质,知道氧气能与铁、氢气、
物质在氧气中燃烧的现象叙述错误的是A.木炭:发出白光B.铁丝:火星四射C.红磷:大量白烟D.硫粉:淡
物质在氧气中燃烧的现象叙述错误的是A.木炭:发出白光B.铁丝:火星四射C.红磷:大量白烟D.硫粉:淡蓝色火焰
02和CO2是动植物生命活动中不可缺少的两种气体 它们的相同点是 ( )A.都能供动植物呼吸
02和CO2是动植物生命活动中不可缺少的两种气体,它们的相同点是 ( )A.都能供动植物呼吸B.都是植物光合作用的原料C.都难溶解于水D.都是空气中的固定成分



 将产生的
将产生的








