为探究一种混合物是由铜粉与镁粉 铁粉 锌粉中的哪一种金属组成。某同学进行了如下实验:称量8.0g该混
| 为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成。某同学进行了如下实验:称量8.0g该混合物粉末放入烧杯中→将140g14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成下图。 |
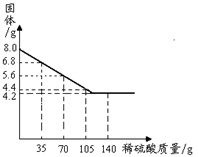 |
| 试计算: ⑴该混合物是由铜粉和____组成的。 ⑵加入105g稀硫酸充分反应后,所得溶液的质量。 |
参考解答
| 解:⑴镁粉 ⑵设生成氢气的质量为x。 Mg+H2SO4==MgSO4+H2↑ 24 2 8.0g-4.4g x 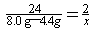 x=0.3g 所得溶液的质量:(8.0g-4.4g)+105g-0.3g=108.3g |
相似问题
NaOH和Ca(OH)2的固体混合物11.4g与118.6gNa2CO3溶液恰好完全反应 过滤后得到
NaOH和Ca(OH)2的固体混合物11 4g与118 6gNa2CO3溶液恰好完全反应,过滤后得到干燥的固体10g。求:(1)Na2CO3溶液中溶质的质量。(2)过滤后所得溶液的溶质质量分数。
为从定量角度认识中和反应 小明同学自行设计并进行了下面实验:①在小烧杯中倒入8%的氢氧化钠溶液10g
为从定量角度认识中和反应,小明同学自行设计并进行了下面实验:①在小烧杯中倒入8%的氢氧化钠溶液10g,滴入2滴酚酞试剂后,溶液呈红色;②另取10%的稀
某工厂化验室用15%氢氧化钠溶液 洗涤一定量石油产品中的残余硫酸 共消耗这种溶液40克 洗涤后的溶液
某工厂化验室用15%氢氧化钠溶液,洗涤一定量石油产品中的残余硫酸,共消耗这种溶液40克,洗涤后的溶液呈中性。则在这一定量的石油产品中含硫酸多少克?
我国目前使用的燃料主要是煤和石油 含有硫的煤燃烧时生成的SO2会污染空气。(1)某火力发电厂每天燃烧
我国目前使用的燃料主要是煤和石油,含有硫的煤燃烧时生成的SO2会污染空气。(1)某火力发电厂每天燃烧含硫1 6%的煤100t,若煤中的硫全部转化为SO2,则该
有一瓶标签破损的稀硫酸 为测定其溶质质量分数 取出20g溶液 加入足量的锌粒。充分反应后 产生的氢气
有一瓶标签破损的稀硫酸,为测定其溶质质量分数,取出20g溶液,加入足量的锌粒。充分反应后,产生的氢气为0 02g。①计算20g溶液中H2SO4的物质的量(根据












