将2.5g碳酸钠 碳酸氢钠和氢氧化钠的固体混合物完全溶解于水 制成稀溶液 然后向该溶液中逐滴加入1m
| 将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示: (1)写出OA段所发生反应的离子方程式______、______. (2)当加入35mL盐酸时,产生CO2的体积为______mL(标准状况). (3)计算原混合物中NaOH的质量及碳酸钠的质量分数______. 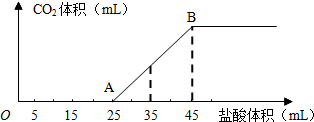 |
参考解答
| (1)在溶液中碳酸氢钠与氢氧化钠反应生成碳酸钠,结合图象可知,开始没有二氧化碳气体生成,则制成的稀溶液中的溶质为碳酸钠和氢氧化钠,则OA段0~5mL先发生酸碱中和, 其离子反应方程式为H++OH-═H2O,再发生碳酸钠与盐酸反应生成碳酸氢钠与氯化钠,其离子反应方程式为CO32-+H+═HCO3-, 故答案为:H++OH-═H2O;CO32-+H+═HCO3-; (2)结合图象可知,当加入35mL盐酸时,25~35mL发生碳酸氢钠与盐酸的反应生成二氧化碳气体, 设生成二氧化碳的物质的量为n,生成气体时消耗的酸的物质的量为(35-25)×10-3L×1mol?L-1=0.01mol,则 HCO3-+H+═CO2↑+H2O 1 1 0.01mol n
故答案为:224; (3)设碳酸钠、碳酸氢钠和氢氧化钠的物质的量分别为x、y、z,则 ①x+y=1mol/L×(0.045-0.025)L ②x+z=1mol/L×0.025L ③84g/mol?x+106g/mol?y+40g/mol?z=2.5g 联立①②③式解得x=0.01mol,y=0.01mol,z=0.015mol 故NaOH的质量为0.015mol×40g/mol=0.6g, Na2CO3的质量分数为
答:原混合物中NaOH的质量为0.6g,碳酸钠的质量分数为42.4%. |
相似问题
下列反应中 不能用离子方程式Ba2++SO42-=BaSO4↓来表示的是 [ ]A 稀硫
下列反应中,不能用离子方程式Ba2++SO42-=BaSO4↓来表示的是[ ]A、稀硫酸溶液与硝酸钡溶液反应B、硫酸钾溶液与氯化钡溶液反应 C、稀硫酸溶液与氢氧化钡
下列离子方程式正确的是[ ]A.将氨水滴入到FeCl3溶液中 Fe3++3OH-===Fe(
下列离子方程式正确的是[ ]A.将氨水滴入到FeCl3溶液中 Fe3++3OH-===Fe(OH)3↓ B.氧化铁与盐酸反应 Fe2O3+6H+===2Fe3++3H2OC.向FeCl3溶液中
下列反应的离子方程式书写中 正确的是( )A.硫酸亚铁酸性溶液置于空气中变质:4Fe2++O2+4
下列反应的离子方程式书写中,正确的是( )A.硫酸亚铁酸性溶液置于空气中变质:4Fe2++O2+4H+=4Fe3++2H2OB.少量稀HNO3中加入足量铁粉:Fe+4H++NO3-=
下列离子方程式正确的是( )A.钠与水反应:Na+2H2O=Na++2OH-+H2↑B.稀硫酸中加
下列离子方程式正确的是( )A.钠与水反应:Na+2H2O=Na++2OH-+H2↑B.稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑C.硫酸铝溶液中加入过量氨水:Al3++3OH
下列离子方程式正确的是( )A.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑B.碳酸钙与稀
下列离子方程式正确的是( )A.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑B.碳酸钙与稀硝酸反应:CO32-+2H+=CO2↑+H2OC.盐酸与氢氧化钡溶液反应:H++OH-












