(10分)五种短周期元素A B C D E 原子序数逐渐增大 A B处于同一周期 C D E同处另一
| (10分)五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E周期序数等于E原子最外层电子数。根据以上信息回答下列问题: (1)A、B、C、D、E五种元素的原子半径由小到大的顺序是 (用元素符号填写) (2)乙物质中存在的化学键类型是 。 (3)选用恰当的试剂除去D中少量的E,写出发生反应的化学方程式 (4)化合物乙的电子式 (5)将D、E的单质插入NaOH溶液中,构成原电池,其负极反应是 |
参考解答
| (1)O<N< Al <Mg< Na;(2)离子键、共价键;(3)2Al+2NaOH+2H2O=2NaAlO2+3H2↑ (4) 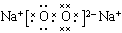 (5)Al-3e-+4OH-=AlO2-+2H2O。 (5)Al-3e-+4OH-=AlO2-+2H2O。 |
试题分析:根据题意可知这五种元素分别是:A是N;B是O;C是Na;D是Mg;E是Al。同一周期的元素,原子序数越大,原子半径就越小;不同周期的元素,原子核外电子层数越多,原子半径就越大。所以这五种元素的原子半径由小到大的顺序是:O<N< Al <Mg< Na ;(2)O、Na形成的原子个数比为1:1的化合物物质乙Na2O2中存在的化学键类型是离子键、共价键;(3)由于Mg、Al都是金属,Al能够与碱反应,而Mg不能发生反应,所以可以用NaOH溶液除去D中少量的E,发生反应的化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑。(4)化合物Na2O2的电子式是 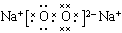 ;(5)若将D、E的单质插入NaOH溶液中,可以构成原电池,由于Al能够与NaOH发生反应,所以Al作负极,其负极反应是Al-3e-+4OH-=AlO2-+2H2O。 ;(5)若将D、E的单质插入NaOH溶液中,可以构成原电池,由于Al能够与NaOH发生反应,所以Al作负极,其负极反应是Al-3e-+4OH-=AlO2-+2H2O。 |
相似问题
下列4组物质均有一种物质的类别与其它3种不同A.CaO Na2O CO2 CuOB.H2 C P C
下列4组物质均有一种物质的类别与其它3种不同A.CaO、Na2O、CO2、CuOB.H2、C、P、CuC.O2、Fe、Cu、ZnD.HCl、H2O、H2SO4、HNO3以上四组物质中与别不同
下列判断正确的是( )A.酸性氧化物一定是非金属氧化物B.只含有一种元素的物质 一定是纯净物C.碱
下列判断正确的是( )A.酸性氧化物一定是非金属氧化物B.只含有一种元素的物质,一定是纯净物C.碱性氧化物一定是金属氧化物D.硫酸、纯碱、石膏分
摩尔盐的组成可用(NH4)2SO4·FeSO4·6H2O表示 下列关于该物质的叙述不正确的是[
摩尔盐的组成可用(NH4)2SO4·FeSO4·6H2O表示,下列关于该物质的叙述不正确的是[ ]A.它是由(NH4)2SO4与FeSO4组成的混合物B.它是一种纯净物C.它是一种
NaOH Na2CO3 NaCl Na2SO4可按某种标准划为一类物质 下列分类标准不正确的是(
NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为一类物质,下列分类标准不正确的是( )A.钠的化合物B.可与硝酸反应C.可溶于水D.电解质
下列物质的分类正确的是 [ ]碱 酸盐碱性氧化物酸性氧化物 A.Na2CO3 H2SO4
下列物质的分类正确的是 [ ]碱酸盐碱性氧化物酸性氧化物 A Na2CO3H2SO4NaOHSO2 CO2 B NaOH HCl NaCl Na2OCO C NaOH CH3COOHCaF2 CO SO2 D KOH HNO3 CaCO3 CaOSO2












