氧化还原反应H2O2+H2CrO4→Cr(OH)3+O2↑+H2O(1)配平并用单线桥标出电子转移方
| 氧化还原反应H2O2+H2CrO4→Cr(OH)3+O2↑+H2O (1)配平并用单线桥标出电子转移方向和数目______. (2)该反应中的还原剂是______,被还原的元素______,发生还原反应的物质______,还原产物是______; (3)反应转移了0.3mol电子,则产生的气体在标准状态下体积约为______. |
参考解答
(1)Cr化合价从+6→+3,得电子,0化合价从-1→0,失电子,因此箭头指向由O指向Cr,电子总数为:2×(6-3)═6.用单线桥法表示反应中电子转移的方向和数目如下: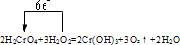 , ,故答案为: 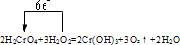 ; ;(2)该反应中失电子化合价升高的反应物是H2O2,得电子化合价降低的元素是
故答案为:H2O2,
(3)根据得失电子守恒得生成氧气的物质的量为
故答案为:3.36L. |
相似问题
(6分)利用氧化还原反应原理配平以下化学方程式 并: FeSO4 + KNO3 + H2SO4
(6分)利用氧化还原反应原理配平以下化学方程式,并: FeSO4 + KNO3 + H2SO4 === K2SO4 + Fe2(SO4)3 + NO↑+ H2O(1)标出电子转移的
下列叙述正确的是( )A.将磁性氧化铁放入稀HNO3中发生如下反应:3Fe3O4+28HNO3﹦9
下列叙述正确的是( )A.将磁性氧化铁放入稀HNO3中发生如下反应:3Fe3O4+28HNO3﹦9Fe(NO3)3+NO↑+14H2O反应中每还原0 2mol氧化剂,就有0 6mol电子
在反应KClO3 + 6HCl='=' KCl +3Cl2↑+3H2O中 被氧化与被还原的氯原子个数
在反应KClO3 + 6HCl= "= " KCl +3Cl2↑+3H2O中,被氧化与被还原的氯原子个数比为()A.1:6B.6:1C.1:5D.5:1
在一定条件下 RO3n- 和氟气可发生如下反应:RO3n- +F2+2OH-==RO4- +2F-+
在一定条件下,RO3n- 和氟气可发生如下反应:RO3n- +F2+2OH-==RO4- +2F-+H2O。从而可知在RO3n-中,元素R的化合价是[ ]A、+4 B、+5 C、+6 D、+7
下列氧化还原反应中电子转移的方向和数目正确的是[ ]A. B. C. D.
下列氧化还原反应中电子转移的方向和数目正确的是[ ]A B C D












