(15分)电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间 通过电解生
(15分)电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示: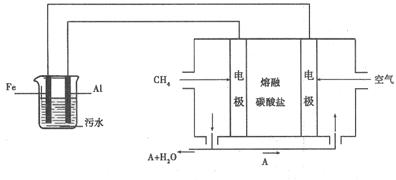 (1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的 。 a.H2SO4 b.BaSO4 c.N2SO4 d.NaOH e.CH3CH2OH (2)电解池阳极的电极反应分别是① ; ② 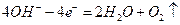 。 。(3)电极反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式是 。 (4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。 已知负极的电极反应是 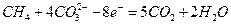 。 。①正极的电极反应是 。 ②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。则A物质的化学式是 。 (5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4  (标准状况) L。 (标准状况) L。 |
参考解答
(1)c 2分 (2)Fe-2e-=Fe2+ 2分 (3)4Fe2++10H2O+O2=4Fe(OH)3↓+8H+ 3分 (4)①O2+2CO2+4e-=2CO32- (2O2+4CO2+8e-=4CO32-) 3分 ②CO2 2分 (5)11.2 3分 |
| 略 |
相似问题
下列微粒①Al3+ ②Cl- ③N2 ④MnO4- ⑤CO2 ⑥H2O2 ⑦Fe2+ ⑧
下列微粒①Al3+②Cl-③N2④MnO4-⑤CO2⑥H2O2⑦Fe2+⑧MnO42-.既具有氧化性又具有还原性的是( )A.①④⑤⑦B.③⑥⑦⑧C.④⑤⑥⑧D.①②③⑥
下列各组物质中 均能使Fe2O3还原成单质铁的是( )A.CO O2 HeB.CO CO2 CC.
下列各组物质中,均能使Fe2O3还原成单质铁的是( )A.CO、O2、HeB.CO、CO2、CC.CO2、H2O、O2D.Al、C、H2
实现下列变化 必须加入氧化剂或还原剂的是 [ ]A.NO2→HNO3 B.NH
实现下列变化,必须加入氧化剂或还原剂的是 [ ]A.NO2→HNO3B.NH4+→NH3C.Cl2→HClOD.NH3→NO
已知下列反应:(1)2A3++2B-====2A2++B2(2)C2+2B-====2C-+B2(3
已知下列反应:(1)2A3++2B-====2A2++B2(2)C2+2B-====2C-+B2(3)2A2++C2====2A3++2C-下列有关物质氧化性、还原性强弱的判断,正确的是()A.氧化性:B2>C2
现有C CO CO2 Na2CO3四种物质 采用下列分类标准 无法将其中两种归为一类的是( )A.
现有C、CO、CO2、Na2CO3四种物质,采用下列分类标准,无法将其中两种归为一类的是( )A.是否具有还原性B.是否为氧化物C.碳元素的化合价是否相同D












