Ⅰ.某实验小组把CO2通入饱和Na2CO3溶液制取NaHCO3 装置如图所示(气密性已检验 部分夹持
Ⅰ.某实验小组把CO2通入饱和Na2CO3溶液制取NaHCO3,装置如图所示(气密性已检验,部分夹持装置略):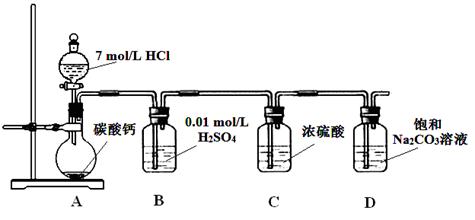 (1)请结合化学平衡移动原理解释B中溶液的作用 。 (2)当D中有大量白色固体析出时,停止实验,将固体过滤、洗涤,取一定量配成样液,并加入BaCl2溶液,出现白色沉淀并有气体产生,其离子方程式是 。 Ⅱ.某课外活动小组欲利用氨气与CuO反应,研究氨气的性质并测其组成,设计了如下实验(夹持装置未画出)进行实验。请回答下列问题: 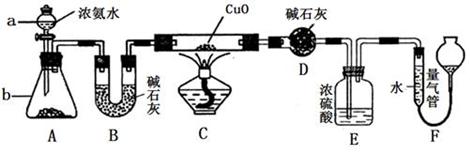 (1)仪器b中可选择的试剂为(任意填一种) 。 (2)实验中,装置C中黑色CuO粉末全部转化为红色固体(已知Cu2O也为红色固体),量气管中有无色无味的气体。实验前称取黑色CuO 80g,实验后得到红色固体质量为68g。则红色固体成分的化学式为 。 (3)F中读取气体体积前,应向上或向下移动右管,使得左右两边液面相平,若无此操作,而F中左边液面低于右边液面,会导致读取的气体体积 (填“偏大”或“偏小”或“无影响”)。 (4)要想测得氨气分子中氮、氢原子个数比,实验中应至少测量或读取哪些数据 (填序号)。 a.B装置实验前后质量差mg; b.F装置实验前后液面差VL c.D装置实验前后质量差mg; d.E装置实验前后质量差mg; (5)E装置中浓硫酸的作用是 。 |
参考解答
Ⅰ.(1)CO2在水中存在平衡:CO2+H2O H2CO3 H2CO3 HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体(3分)[给分要点:吸收HCl气体、减少CO2在水中的溶解、H2SO4电离出的H+使平衡左移 HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体(3分)[给分要点:吸收HCl气体、减少CO2在水中的溶解、H2SO4电离出的H+使平衡左移(2)2HCO3-+Ba2+=BaCO3↓+ CO2↑+H2O(3分) Ⅱ.(1)碱石灰或生石灰或氢氧化钠固体(任意填一种)(2分) (2)Cu和Cu2O(3分) (3)偏小(2分) (4)b、c(3分) (5)防止F中水蒸气进入D中,并吸收氨气(2分) |
试题分析:Ⅰ.(1)7mol?L ̄1的盐酸与CaCO3反应制取的CO2气体中含有HCl,硫酸溶液可吸收HCl,CO2能溶于水,存在平衡::CO2+H2O  H2CO3 H2CO3 HCO3-+H+,H2SO4电离产生H+,使上述平衡向左移动,从而减少CO2在水中的溶解。 HCO3-+H+,H2SO4电离产生H+,使上述平衡向左移动,从而减少CO2在水中的溶解。(2)当D中有大量白色固体析出时,CO2、H2O与Na2CO3反应生成了NaHCO3,加入BaCl2溶液,出现白色沉淀为BaCO3,产生的气体为CO2,离子方程式为:2HCO3-+Ba2+=BaCO3↓+ CO2↑+H2O Ⅱ.(1)碱石灰或生石灰或氢氧化钠固体都能与浓氨水作用,产生氨气。 (2)若CuO全部被还原为Cu,根据关系式:CuO ~ Cu,生成的Cu质量为:80g×64/80=64g;若CuO全部被还原为Cu2O,根据关系式:2CuO ~ Cu2O,生成的Cu2O质量为:80g×144/160=72g,实际得到红色固体质量为68g,则红色固体成分为Cu和Cu2O (3)F中左边液面低于右边液面,说明左边气体压强大于右边,则会导致读取的气体体积偏小。 (4)F装置实验前后液面差VL,为NH3与CuO反应生成的N2的体积,可求出N原子的物质的量,D装置实验前后质量差mg,为NH3与CuO反应生成的H2O的质量,可求出H原子的物质的量,由二者可求出氨气分子中氮、氢原子个数比。 (5)因为D中碱石灰的作用是吸收NH3与CuO反应生成的H2O,所以E中浓硫酸可F中水蒸气进入D中,并吸收未反应的氨气。 |
相似问题
向CuSO4的溶液中投入一小块金属钠 可观察到的现象是[ ]A.有较多的铜析出 B.有气
向CuSO4的溶液中投入一小块金属钠,可观察到的现象是[ ]A.有较多的铜析出 B.有气体产生 C.有蓝色沉淀产生 D.有白色沉淀产生
纯碱(Na2CO3) 在生产生活中具有广泛的用途。以下是实验室模拟制碱原理制取Na2CO3的流程图:
纯碱(Na2CO3) 在生产生活中具有广泛的用途。以下是实验室模拟制碱原理制取Na2CO3的流程图:已知:向饱和食盐水中通入NH3、CO2后发生的反应为NaCl+NH3+CO
下列关于物质应用的说法错误的是A.玻璃容器可长期盛放各种酸B.纯碱可用于清洗油污C.浓氨水可检验氯气
下列关于物质应用的说法错误的是A.玻璃容器可长期盛放各种酸B.纯碱可用于清洗油污C.浓氨水可检验氯气管道漏气D.Na2S可除去污水中的Cu2+
下列说法不正确的是 [ ]A.由于高压钠灯发出的黄光射程远 透雾力强 钠常应用于电光源B.铝
下列说法不正确的是 [ ]A.由于高压钠灯发出的黄光射程远,透雾力强,钠常应用于电光源B.铝易与空气中的氧气起反应,但由于生成的氧化膜致密,可以保
等质量的两块钠 第一块在足量氧气中加热 第二块在足量氧气(常温)中充分反应 则下列说法正确的是[
等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则下列说法正确的是[ ]A.第一块钠失去电子多B.两块钠失去电子一样多












