在如图所示的装置中 锥形瓶中装有饱和石灰水 小试管中装有一定量的水 气球中有一小块用铝箔包着的钠 整
| 在如图所示的装置中,锥形瓶中装有饱和石灰水,小试管中装有一定量的水,气球中有一小块用铝箔包着的钠,整套装置气密性良好,未反应前U形管两端液面相平.现将气球中的金属钠放入小试管中与水反应. (1)观察到的现象是:①______;②______;③______. (2)产生上述现象的原因是______. (3)写出钠与水反应的离子方程式______. 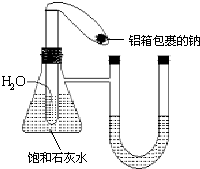 |
参考解答
| (1)金属钠和水的反应生成氢氧化钠和氢气,该是放热的,而饱和石灰水的溶解度随温度升高而降低,所以会析出晶体,变浑浊,同时气体具有热胀冷缩的性质,锥形瓶中气压增大,导致U形管中液面变化, 故答案为:①有气体产生,是气球膨胀;②U型管右边液面上升,左边液面下降;③饱和石灰水中会有沉淀生成; (2)金属钠和水的反应生成氢氧化钠和氢气,该是放热的,而饱和石灰水的溶解度随温度升高而降低,所以会析出晶体,变浑浊,同时气体具有热胀冷缩的性质,锥形瓶中气压增大,导致U形管中液面的变化, 故答案为:钠与水反应产生氢气会使气球膨胀;同时又热量放出,使周围空气膨胀,则U型管左边液面下降,右边液面上升;由于Ca(OH)2的溶解度随温度的升高而降低,则有沉淀产生. (3)金属钠和水反应的实质是:2Na+2H2O=2Na++2OH-+H2↑, 故答案为:2Na+2H2O=2Na++2OH-+H2↑. |
相似问题
将一定量的钠铝合金置于水中 合金全部溶解 得到20mL OH-浓度为1mol/L的溶液 然后用1mo
将一定量的钠铝合金置于水中,合金全部溶解,得到20mLOH-浓度为1mol L的溶液,然后用1mol L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选
下列对有关物质性质的分析正确的是( )A.Na久置于空气中 可以和空气中的有关物质反应 最终生成N
下列对有关物质性质的分析正确的是( )A.Na久置于空气中,可以和空气中的有关物质反应,最终生成NaHCO3B.在高温下用氢气还原MgCl2可制取金属镁C.
甲 乙 丙 丁四个烧杯内分别放入0.1mol的钠 氧化钠 过氧化钠和氢氧化钠 然后各加入100mL水
甲、乙、丙、丁四个烧杯内分别放入0 1mol的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体完全溶解,则甲、乙、丙、丁的质量分数大小
如图表示由元素周期表中1~20号且不同主族元素组成的单质及化合物之间转化关系(产物中的水已略去)。其
如图表示由元素周期表中1~20号且不同主族元素组成的单质及化合物之间转化关系(产物中的水已略去)。其中A为单质;在实验室中,常用固体B和固体C加热制
下列关于钠的叙述中 不正确的是( )A.钠是硬度很大的银白色金属B.钠燃烧时 发出黄色的火焰C.钠
下列关于钠的叙述中,不正确的是( )A.钠是硬度很大的银白色金属B.钠燃烧时,发出黄色的火焰C.钠在空气中燃烧时,生成淡黄色固体D.钠原子最外层












