已知A B D E四种物质中均含有同一种短周期元素 该元素原子的最外层电子数是内层电子数的3倍 D为
已知A、B、D、E四种物质中均含有同一种短周期元素,该元素原子的最外层电子数是内层电子数的3倍,D为气体单质,E为黑色粉末.如图转化关系中E均起催化作用(某些产物已略去).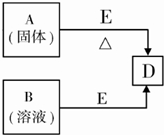 则: (1)A的化学式为______;B分子的电子式为______; (2)已知E与含A中某元素的浓酸在一定条件下反应,产生一种含有该元素的气体X.甲同学为探究该气体的性质,设计了如图装置(III中夹持装置已略去). 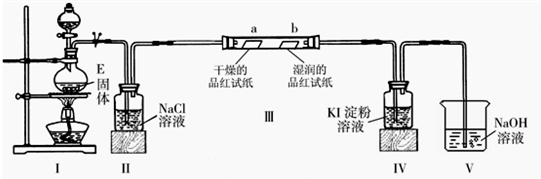 ①I中发生反应的离子方程式为______; ②实验开始不久,观察到装置IV中的现象为______; ③实验结束后,该同学在装置III中观察到b的红色褪去,而没有出现“a无明显现象”这一预期现象.为达到实验目的,他在装置______(填装置序号)之间又添加了洗气瓶,该装置的作用是______; (3)将气体X通入到紫色的石蕊试液中,观察到的现象是______; (4)气体X能与溶液B反应,生成气体D,试写出该反应的化学方程式:______. |
参考解答
| 已知A、B、D、E四种物质中均含有同一种短周期元素,该元素原子的最外层电子数是内层电子数的3倍,应为O元素,D为气体单质,应为O2,E为黑色粉末,应为MnO2,根据物质的状态和反应条件下可知A为KClO3,B为H2O2,都可在MnO2作用下生成氧气,E与含A中某元素的浓酸在一定条件下反应,产生一种含有该元素的气体X,应为MnO2与浓盐酸的反应,生成X为Cl2, (1)由以上分析可知A为KClO3,B为H2O2,电子式为 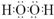 ,故答案为:KClO3; 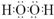 ; (2)①Ⅰ为制取氯气的发生装置,反应的方程式为MnO2+4H++2Cl-
故答案为:MnO2+4H++2Cl-
②氯气具有氧化性,与KI反应生成碘单质,淀粉遇碘变蓝色,故答案为:溶液变蓝; ③为验证干燥的氯气不具有漂白性,则通入Ⅲ中的氯气应为干燥后的氯气,应装置II和III添加盛有浓硫酸的洗气装置,用以除去氯气中的水蒸气, 故答案为:装置II和III;除去氯气中的水蒸气(或:干燥氯气); (3)氯气与水反应生成盐酸和次氯酸,次氯酸具有漂白性,可使紫色的石蕊试液先变红后褪色,故答案为:紫色的石蕊试液先变红后褪色; (4)气体Cl2能与溶液H2O2反应,生成气体O2,该反应的方程式为Cl2+H2O2=2HCl+O2,故答案为:Cl2+H2O2=2HCl+O2. |
相似问题
能实现下列物质间直接转化的元素是( )单质+O2氧化物+H2O酸或碱 +NaOH或HCl 盐.A.
能实现下列物质间直接转化的元素是( )单质+O2氧化物+H2O酸或碱 +NaOH或HCl盐.A.硅B.硫C.铜D.铁
如图所示 已知:①甲 乙 丙均为前三周期元素的气体单质 丁为固体单质.②在一定条件下甲与丙 甲与丁都
如图所示,已知:①甲、乙、丙均为前三周期元素的气体单质,丁为固体单质.②在一定条件下甲与丙、甲与丁都按微粒个数比l:3组成X和Y,在产物中元素甲呈
A B C D E五种物质中含有同一种元素 其相互转化关系如图所示.其中A B C D在常温下都是气
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D在常温下都是气体,B为红棕色.(1)写出各下列物质的化学式:则A是___
A B C分别是三种常见单质;D E F则是常见的三种氧化物 且有如图所示转化关系 下列说法错误的是
A、B、C分别是三种常见单质;D、E、F则是常见的三种氧化物,且有如图所示转化关系,下列说法错误的是( )A.B可能是金属B.A、B、C中肯定有O2C.D中
A单质是实验室用来处理汞污染的常用试剂 其元素在周期表中的族序数是周期数的两倍.乙在常温下是无色 无
A单质是实验室用来处理汞污染的常用试剂,其元素在周期表中的族序数是周期数的两倍.乙在常温下是无色、无味的液体,电解是能产生两种状态一样的气体,甲












