将一块钠用小刀切开 暴露在空气中 可以观察到如下现象:(1)金属钠表面变暗。(2)过一会又变潮湿 同
| 将一块钠用小刀切开,暴露在空气中,可以观察到如下现象: (1)金属钠表面变暗。 (2)过一会又变潮湿,同时使用放大镜观察,发现多处有小气泡生成。 (3)再过较长时间又转变为白色晶体。 (4)白色晶体最终变成白色粉末。 试写出上述反应现象的有关化学方程式。 |
参考解答
(1)4Na+O2 2Na2O 2Na2O(2)Na2O+H2O  2NaOH 2NaOH2H2O+2Na2  NaOH+H2↑ NaOH+H2↑(3)2NaOH+CO2+9H2O  Na2CO3·10H2O Na2CO3·10H2O(4)Na2CO3·10H2O 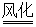 Na2CO3+10H2O Na2CO3+10H2O |
| 钠表面变暗,是因为钠与空气中的氧气反应生成氧化钠。氧化钠易与空气中的水反应生成氢氧化钠,而氢氧化钠易与空气中的CO2反应生成Na2CO3和H2O;由于钠与水接触反应,生成的氢气从溶液中逸出而形成许多小气泡。NaOH溶液易吸收空气中的二氧化碳生成碳酸钠,碳酸钠在水溶液中以Na2CO3·10H2O形式结晶析出。由于Na2CO3·10H2O在干燥空气中易风化,故再过一段时间,Na2CO3·10H2O失去结晶水变为粉末状碳酸钠。 |
相似问题
合乎实际并应用于工业生产的是 (
合乎实际并应用于工业生产的是()A.金属钠在氯气中燃烧制氯化钠 B.氢气和氯气混合后经光照制氯化氢C.氯气和澄清石灰水作用制漂白粉D.浓硫酸和莹石
将100gK2CO3和KHCO3的混合物加热至质量不再变化时 共收集到CO211g 原混合物中KHC
将100gK2CO3和KHCO3的混合物加热至质量不再变化时,共收集到CO211g,原混合物中KHCO3的质量分数是()A.30% B.40% C.50% D.60%
将一小块钠放在石棉网上加热 下列组合正确的是( )①燃烧 黄色火星四射②金属熔化③燃烧火焰为黄
将一小块钠放在石棉网上加热,下列组合正确的是( )①燃烧,黄色火星四射②金属熔化③燃烧火焰为黄色④燃烧生成白色固体⑤燃烧生成淡黄色固体A.②①B.
将0.5 mol钠与0.5 mol镁分别加入2 mol·L-1 400 mL的硫酸中 所得溶液的质量
将0 5 mol钠与0 5 mol镁分别加入2 mol·L-1、400 mL的硫酸中,所得溶液的质量是A.硫酸钠溶液的质量大B.同样大C.硫酸镁溶液的质量大D.无法确定
钾的金属活动性比钠强 根本原因是( )A.钾的密度比钠的小B.钾原子的电子层比钠原子多一层C.钾与水
钾的金属活动性比钠强,根本原因是()A.钾的密度比钠的小B.钾原子的电子层比钠原子多一层C.钾与水反应比钠与水反应更剧烈D.加热时,钾比钠更易汽化












