向某NaOH溶液中通入CO2气体后得到溶液M 因CO2通入的量不同 溶液M的组成也不同 若向M中逐滴
向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如下图所示。则下列分析与判断不正确的是(不计CO2的溶解) ( )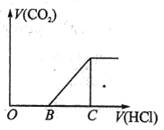
|
参考解答
| C |
| 向Na2CO3溶液中逐滴加入盐酸,反应原理为: Na2CO3+HCl=NaCl+NaHCO3,NaHCO3+HCl=NaCl+CO2+H2O,即从Na2CO3到NaHCO3所消耗盐酸的量相等。对A,若OA=0,表明开始滴加盐酸就有气体生成,则M中的溶质NaHCO3,反应为CO2+OH—=HCO3—;对B,若OB=BC,说明生成HCO3—消耗的H+与HCO3—产生CO2消耗的H+相等,则M中的溶质为Na2CO3;对C,OB>BC,说明不产生CO2消耗H+大于产生CO2消耗的H+量,M中溶质应为NaOH和Na2CO3,若OB<BC,说明不产生CO2消耗H+小于产生CO2消耗的H+量,M中溶质应为Na2CO3和NaHCO3;对D,3OB=BC,M中溶质为Na2CO3和NaHCO3,因为Na2CO3~NaHCO3,故c(NaHCO3=2c(Na2CO3)。 |
相似问题
溴化碘(IBr)的化学性质与卤素单质相似 它和水反应的化学方程式:IBr+H2O H
溴化碘(IBr)的化学性质与卤素单质相似,它和水反应的化学方程式:IBr+H2OHBr+HIO。则下列关于IBr的叙述中不正确的是()A.IBr是共价化合物B.在很多反
已知氯化碘(ICl)的性质类似于卤素 有很强的化学活性。ICl跟Zn H2O分别发生如下反应:2IC
已知氯化碘(ICl)的性质类似于卤素,有很强的化学活性。ICl跟Zn、H2O分别发生如下反应:2ICl+2ZnZnCl2+ZnI2,ICl+H2OHCl+HIO,下列叙述正确的是()A
根据下图所示的A B C D E 五种物质的相互转化关系 按如下关系填写相应的物质和有关反应的化学方
根据下图所示的A、B、C、D、E 五种物质的相互转化关系,按如下关系填写相应的物质和有关反应的化学方程式:(1)当A是气体单质时,B是_________,C是___
如右图是一套实验室制取气体的装置。某课外活动小组利用这套装置快速制取Cl2 HCl和O2。供选用的试
如右图是一套实验室制取气体的装置。某课外活动小组利用这套装置快速制取Cl2、HCl和O2。供选用的试剂有:A.浓H2SO4B.浓盐酸C.食盐D.二氧化锰 E KMnO
实验室制取氯气 常用排饱和食盐水的方法收集 原因是A.可产生更多的氯气B.只有饱和食盐水才能除去HC
实验室制取氯气,常用排饱和食盐水的方法收集,原因是A.可产生更多的氯气B.只有饱和食盐水才能除去HCl杂质C.既能除去HCl,又能防止Cl2的溶解D.食盐水易得到












