如下图所示 把试管放入盛有25℃澄清饱和石灰水的烧杯中 试管中开始放入几块镁条 再用滴管滴入5mL的
如下图所示,把试管放入盛有25℃澄清饱和石灰水的烧杯中,试管中开始放入几块镁条,再用滴管滴入5mL的盐酸于试管中。试回答下列问题: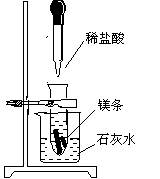 ⑴实验中观察到的现象有 。 ⑵产生上述实验现象的原因是 。 ⑶写出有关的离子方程式 。 ⑷由实验可知,MgCl2和H2的总能量 (填“大于”、“小于”或“等于”)镁条和盐酸的总能量。 ⑸如将本题中“25℃澄清饱和石灰水”换成“20℃的碳酸饮料”进行探究实验,实验中观察到的另一现象是 。其原因是 。 |
参考解答
| ⑴镁条上产生大量的气泡,镁条逐渐溶解,烧杯中析出白色固体(或溶液变浑浊) ⑵镁与盐酸反应产生H2,且该反应是放热反应,而Ca(OH)2的溶解度随着温度的升高而减小,因此析出白色的Ca(OH)2固体⑶ Mg + 2H+= Mg2++ H2↑⑷小于⑸烧杯中的液体放出气泡。气体的溶解度随着温度的升高而减小。 |
| 本题考查金属镁与盐酸反应为放热反应、石灰水的溶解度受温度的影响的反常现象以及二氧化碳的溶解度问题。 |
相似问题
下列变化中 不需要破坏化学键的是( )A.碘升华B.氯酸钾分解C.氯化氢溶于水D.石墨转变为金刚石
下列变化中,不需要破坏化学键的是( )A.碘升华B.氯酸钾分解C.氯化氢溶于水D.石墨转变为金刚石
下列说法不正确的是( )A.放热反应在常温下一定很容易发生B.反应是吸热还是放热 是由反应物和生
下列说法不正确的是( )A.放热反应在常温下一定很容易发生B.反应是吸热还是放热,是由反应物和生成物所具有的总能量相对大小决定的,而与反应条件无关C
下列物质中 化学键类型完全相同的是( )A.H2O和NaFB.N2和NaClC.Na2O和NaCl
下列物质中,化学键类型完全相同的是( )A.H2O和NaFB.N2和NaClC.Na2O和NaClD.CH4和Na2CO3
化学键的断裂和形成的观点不能用于解释下列化学事实中的( )A.氧化还原反应B.化学反应的能量变化C
化学键的断裂和形成的观点不能用于解释下列化学事实中的( )A.氧化还原反应B.化学反应的能量变化C.加成反应D.化学反应过程的本质
下列说法正确的是( )A.化学键断裂放出能量B.离子化合物中可能含有共价键C.单质中可能含离子键D
下列说法正确的是( )A.化学键断裂放出能量B.离子化合物中可能含有共价键C.单质中可能含离子键D.由分子组成的物质中一定存在共价键












