(7分)(1)在配合物Fe(SCN)2+中提供空轨道接受孤电子对的微粒是 (填符号) 画
(7分)(1)在配合物Fe(SCN)2+中提供空轨道接受孤电子对的微粒是 (填符号),画出配合物离子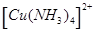 中的配位键 。 中的配位键 。(2)根据价层电子对互斥理论,H30+中VSEPR模型名称为 ,BCl3分子的立体结构为 。 (3)按要求写出由第二周期元素为中心原子,通过SP3杂化形成中性分子的化学式(各写一种):正四面体分子 ,三角锥形分子 ,V型分子 。 |
参考解答
(7分)(1) Fe3+ 1分 ,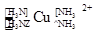 1分。 1分。(2)正四面体 1分,正三角形(平面三角形)1分。 (3)CH4或CF4 1分, NH3或NF3 1分, H2O 1分 |
(1)提供空轨道接受孤电子对的微粒是Fe3+。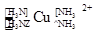 (2) H30+中VSEPR模型名称为正四面体,BCl3分子的立体结构为正三角形 (3)举例:正四面体分子:CH4, 三角锥形分子NH3, V型分子:H2O |
相似问题
(11分)2-1 画出2 4-戊二酮的钠盐与Mn3+形成的电中性配合物的结构式(配体用表示)。2-2
(11分)2-1 画出2,4-戊二酮的钠盐与Mn3+形成的电中性配合物的结构式(配体用表示)。2-2 已知该配合物的磁矩为4 9玻尔磁子,配合物中Mn的未成对电子数
下列对有关微粒结构的表示或说法不正确的是
下列对有关微粒结构的表示或说法不正确的是()A.氮分子的电子式为::N:::N:B.氨分子的空间构型为三角锥型,属于极性分子C.白磷属于分子晶体,空间构
下列物质中 属于共价化合物的是A.Na2CO3B.NH4ClC.H2SD.O2
下列物质中,属于共价化合物的是A.Na2CO3B.NH4ClC.H2SD.O2
(6分) 有下列各组微粒 物质:①金刚石 石墨 ② CH3-O-CH3 CH3-CH2-OH ③
(6分) 有下列各组微粒、物质:①金刚石、石墨② CH3-O-CH3、CH3-CH2-OH③16O、18O④ CH3-CH2-CH =CH2、CH3-CH=CH-CH3⑤ O2、O3⑥12C、13C。其中
下列对化学知识概括合理的是A.两种元素构成的共价化合物分子中的化学键都是极性键B.含有非极性键的化合
下列对化学知识概括合理的是A.两种元素构成的共价化合物分子中的化学键都是极性键B.含有非极性键的化合物一定是共价化合物C.只要是离子化合物,其熔点












