(1)过渡金属离子与水分子形成的配合物是否有颜色 与其d轨道电子排布有关.一般地 d0或d10排布时
| (1)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,d0或d10排布时,无颜色,d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]2+______颜色(填“有”“无”). (2)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.COCl2分子的结构式为 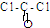 ,则COCl2分子内含有______. A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3个σ键、1个π键. |
参考解答
| (1)Mn2+离子的原子核外排布式为1s22s22p63s23p63d5,其d轨道上有5的电子,故[Mn(H2O)62+ 有颜色, 故答案为:有; (2)COCl2分子的结构式为: 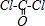 ,C=O键中含有1个δ键,1个π键,则COCl2分子内含有3个σ键、1个π键,故答案为 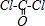 ,D. |
相似问题
下列各组物质的熔沸点按由低到高的顺序排列正确的是A.冰 干冰 氯化钠 金刚石B.汞 钠 烧碱 二氧化
下列各组物质的熔沸点按由低到高的顺序排列正确的是A.冰、干冰、氯化钠、金刚石B.汞、钠、烧碱、二氧化硅C.NaCl、KCl、CsClD.H2O、H2S、H2Se、H2Te
生物质能是一种洁净 可再生能源。生物质气(主要成分为CO CO2 H2等)与H2混合 催化合成甲醇是
生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。(1)上述反应的催化剂含有Cu
Q R X Y Z五种元素的原子序数依次递增。已知:①Z的原子序数为29 其余的均为短周期主族元素;
Q、R、X、Y、Z五种元素的原子序数依次递增。已知:①Z的原子序数为29,其余的均为短周期主族元素;②Y原子价电子(外围电子)排布msnmpn ③R原子核外L层
下列与H2O分子空间构型不相同的是[ ]A.H2SB.NH3C.H2SeD.CO2
下列与H2O分子空间构型不相同的是[ ]A H2SB NH3C H2SeD CO2
在照相底片定影时 硫代硫酸钠(Na2S2O3)溶液能溶解掉未起反应的溴化银 这是因为银离子与硫代硫
在照相底片定影时,硫代硫酸钠(Na2S2O3)溶液能溶解掉未起反应的溴化银,这是因为银离子与硫代硫 酸根离子生成配离子。银离子的配位数为2,若硫代硫酸钠












