1)图3-16为干冰的晶胞结构 观察图形 确定在干冰中每个CO2分子周围有__________个与之
1)图3-16为干冰的晶胞结构,观察图形,确定在干冰中每个CO2分子周围有__________个与之紧邻且等距离的CO2分子。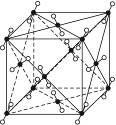 图3-16 在干冰中撒入镁粉,用红热的铁棒引燃后,再盖上另一块干冰,出现的现象为___________ _________,反应的化学方程式是______________________________。 (2)下列三种晶体①CO2 ②CS2 ③SiO2的熔点由高到低的顺序是__________>__________>__________(用序号填空),其原因是______________________________。 |
参考解答
| (1)12 镁粉在干冰中继续燃烧,发出耀眼的白光,并有黑色物质生成 2Mg + CO2  2MgO + C 2MgO + C(2)③ ② ① SiO2是原子晶体,CO2、CS2是分子晶体,所以SiO2熔点最高;CO2和CS2组成和结构相似,且CS2的相对分子质量大于CO2的相对分子质量,所以CS2的熔点高于CO2 |
| (1)以晶胞中的任意一个顶点为坐标原点,以通过该顶点的三条棱边为坐标轴建立起一个三维直角坐标系,在坐标原点的周围可以无隙并置8个晶胞,这样在每一个坐标轴上都可以看到有两个与坐标原点上的CO2分子等距离的CO2分子,但是这些CO2分子与坐标原点上的CO2分子的距离并不是最近的。与坐标原点上的CO2分子最近的CO2分子应该是每一个晶胞的面心上的,共有12个这样的CO2分子。 (2)一般来说,原子晶体的熔点高于分子晶体的熔点,因为原子晶体熔化时要破坏共价键,而分子晶体熔化时只是克服分子间作用力,分子间作用力比共价键弱得多。如果同为分子晶体,当分子的组成和结构相似时,相对分子质量越大,分子间作用力越大,熔沸点越高。 |
相似问题
下列叙述中 错误的是( )A.离子化合物中可能含有非极性键B.分子晶体中不含离子键C.原子晶
下列叙述中,错误的是()A.离子化合物中可能含有非极性键B.分子晶体中不含离子键C.原子晶体中可能含有非极性键D.分子晶体中一定有共价键
(1)通过非极性键形成原子晶体的是_______。(2)固态时属于分子晶体的是_______。(3)
(1)通过非极性键形成原子晶体的是_______。(2)固态时属于分子晶体的是_______。(3)属于分子晶体,且分子为直线型的是_______。(4)由单原子分子构成的分子
下列物质按熔点从低到高顺序排列的是A.O2 Na NaCl SiB.O2 NaCl Na SiC.N
下列物质按熔点从低到高顺序排列的是A.O2 Na NaCl SiB.O2 NaCl Na SiC.Na O2 Si NaClD.Na NaCl SiO2
下列说法中正确的是( )A.NO2 SO2 BF3 NCl3分子中没有一个分子中原
下列说法中正确的是( )A.NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8e-稳定结构B.P4和CH4都是正四面体分子且键角都为109o28
(1)下图为CO2分子晶体结构的一部分。观察图形 试说明每个CO2分子周围有
(1)下图为CO2分子晶体结构的一部分。观察图形,试说明每个CO2分子周围有个与之紧邻等距的CO2分子。(2)试判断:①CO2、②CS2、③SiO2晶体的沸点由高












